MacroArray ALLERGY XPLORER การวินิจฉัยมาโครอาร์เรย์
ข้อมูลจำเพาะ
- ชื่อสินค้า : Basic UDI-DI 91201229202JQ
- หมายเลขอ้างอิง : REF 02-2001-01, 02-5001-01
- การใช้งานที่ตั้งใจไว้: การตรวจจับ IgE เฉพาะสารก่อภูมิแพ้ (sIgE) ในเชิงปริมาณ และ IgE ทั้งหมด (tIgE) ในเชิงกึ่งปริมาณ
- ผู้ใช้งาน: บุคลากรห้องปฏิบัติการที่ผ่านการฝึกอบรมและผู้เชี่ยวชาญทางการแพทย์ในห้องปฏิบัติการทางการแพทย์
- การจัดเก็บ: น้ำยาชุดทดสอบจะคงตัวเป็นเวลา 6 เดือนหลังจากเปิดใช้
คำแนะนำการใช้ผลิตภัณฑ์
หลักการดำเนินการ
ผลิตภัณฑ์ตรวจวัด IgE เฉพาะสารก่อภูมิแพ้ในเชิงปริมาณ และตรวจวัด IgE รวมแบบกึ่งเชิงปริมาณ
การขนส่งและการเก็บรักษา
ตรวจสอบให้แน่ใจว่าได้จัดเก็บชุดน้ำยาตามที่ระบุ และใช้ภายใน 6 เดือนหลังจากเปิดใช้
การกำจัดขยะ:
ปฏิบัติตามขั้นตอนการกำจัดขยะอย่างถูกต้องตามข้อบังคับ
ส่วนประกอบของชุด
ดูคู่มือผู้ใช้สำหรับข้อมูลโดยละเอียดเกี่ยวกับส่วนประกอบของชุด
อุปกรณ์ที่ต้องมี
การวิเคราะห์ด้วยตนเอง: ตรวจสอบให้แน่ใจว่าคุณมีอุปกรณ์ที่จำเป็นซึ่งจัดทำโดยผู้ผลิต
การวิเคราะห์อัตโนมัติ: ใช้เครื่อง MAX, น้ำยาล้าง, น้ำยาหยุดการทำงาน, ซอฟต์แวร์วิเคราะห์ RAPTOR SERVER และพีซี/แล็ปท็อป ปฏิบัติตามคำแนะนำในการบำรุงรักษาอย่างเคร่งครัด
การจัดการอาร์เรย์
ปฏิบัติตามคำแนะนำที่ให้ไว้สำหรับการจัดการอาร์เรย์อย่างระมัดระวังเพื่อให้แน่ใจว่าได้รับผลลัพธ์ที่ถูกต้อง
คำเตือนและข้อควรระวัง
- สวมอุปกรณ์ป้องกันที่เหมาะสม เช่น อุปกรณ์ป้องกันมือและดวงตา และเสื้อคลุมห้องแล็บ
- จัดการสารเคมีและสampและปฏิบัติตามแนวปฏิบัติที่ดีในห้องปฏิบัติการ
- ปฏิบัติต่อแหล่งที่มาของมนุษย์ทั้งหมดเสมือนว่ามีความเสี่ยงต่อการติดเชื้อ และจัดการด้วยความระมัดระวัง
คำถามที่พบบ่อย
- ถาม: สารเคมีในชุดทดสอบมีความคงตัวได้นานเพียงใด?
A: สารเคมีชุดทดสอบจะคงตัวเป็นเวลา 6 เดือนหลังจากเปิดกล่องเมื่อเก็บรักษาภายใต้เงื่อนไขที่ระบุ - ถาม: ใครสามารถใช้ผลิตภัณฑ์นี้ได้บ้าง?
A: ผลิตภัณฑ์นี้มีไว้สำหรับใช้โดยบุคลากรห้องปฏิบัติการที่ได้รับการฝึกอบรมและผู้เชี่ยวชาญทางการแพทย์ในห้องปฏิบัติการทางการแพทย์
www.madx.com
คำแนะนำการใช้งาน ALLERGY XPLORER (ALEX²)
คำอธิบาย
Allergy Xplorer (ALEX²) เป็นการทดสอบการวินิจฉัยในหลอดทดลองโดยใช้ Enzyme-Linked Immunosorbent Assay (ELISA) สำหรับการวัดปริมาณ IgE ที่จำเพาะต่อสารก่อภูมิแพ้ (sIgE) เชิงปริมาณ
คำแนะนำการใช้งานนี้ใช้ได้กับผลิตภัณฑ์ต่อไปนี้:
| UDI-DI พื้นฐาน | อ้างอิง | ผลิตภัณฑ์ |
| 91201229202เจคิว | 02-2001-01 | ALEX² สำหรับการวิเคราะห์ 20 รายการ |
| 02-5001-01 | ALEX² สำหรับการวิเคราะห์ 50 รายการ |
วัตถุประสงค์ที่ตั้งใจ
ALEX² Allergy Xplorer คือชุดทดสอบที่ใช้สำหรับการตรวจซีรั่มหรือพลาสมาของมนุษย์ในหลอดทดลอง (ยกเว้นพลาสมา EDTA) เพื่อให้ข้อมูลในการช่วยวินิจฉัยผู้ป่วยที่เป็นโรคที่เกี่ยวข้องกับ IgE ร่วมกับการตรวจทางคลินิกอื่นๆ หรือผลการทดสอบวินิจฉัย
อุปกรณ์ทางการแพทย์ IVD ตรวจหา IgE เฉพาะสารก่อภูมิแพ้ (sIgE) ในเชิงปริมาณและ IgE รวม (tIgE) ในเชิงกึ่งปริมาณ ผลิตภัณฑ์นี้ใช้โดยบุคลากรห้องปฏิบัติการที่ผ่านการฝึกอบรมและผู้เชี่ยวชาญทางการแพทย์ในห้องปฏิบัติการทางการแพทย์
บทสรุปและคำอธิบายการทดสอบ
อาการแพ้เป็นปฏิกิริยาไวเกินชนิดที่ 1 ที่เกิดขึ้นทันที และเกิดจากแอนติบอดีที่อยู่ในกลุ่ม IgE ของอิมมูโนโกลบูลิน หลังจากได้รับสารก่อภูมิแพ้บางชนิดแล้ว การปล่อยฮีสตามีนและสารก่อภูมิแพ้อื่นๆ จากมาสต์เซลล์และเบโซฟิลที่เกิดจาก IgE จะส่งผลให้เกิดอาการทางคลินิก เช่น หอบหืด เยื่อบุตาอักเสบจากภูมิแพ้ กลาก และอาการทางระบบทางเดินอาหาร [2] ดังนั้น รูปแบบการแพ้ที่ละเอียดต่อสารก่อภูมิแพ้บางชนิดจึงช่วยในการประเมินผู้ป่วยโรคภูมิแพ้ได้ [6-XNUMX] ไม่มีข้อจำกัดเกี่ยวกับกลุ่มประชากรที่ทดสอบ เมื่อทำการทดสอบ IgE โดยทั่วไปจะไม่ถือว่าอายุและเพศเป็นปัจจัยสำคัญ เนื่องจากระดับ IgE ซึ่งวัดได้ในการทดสอบเหล่านี้ไม่แตกต่างกันอย่างมีนัยสำคัญตามกลุ่มประชากรเหล่านี้
ALEX² ครอบคลุมแหล่งสารก่อภูมิแพ้ประเภท I ที่สำคัญทั้งหมด สามารถดูรายการสารสกัดสารก่อภูมิแพ้และสารก่อภูมิแพ้ระดับโมเลกุลของ ALEX² ได้ที่ส่วนท้ายของคำแนะนำนี้
ข้อมูลสำคัญสำหรับผู้ใช้!
สำหรับการใช้งาน ALEX² อย่างถูกต้อง ผู้ใช้จะต้องอ่านและปฏิบัติตามคำแนะนำการใช้งานเหล่านี้อย่างละเอียดถี่ถ้วน ผู้ผลิตจะไม่รับผิดชอบต่อการใช้งานระบบทดสอบนี้ที่ไม่ได้อธิบายไว้ในเอกสารนี้ หรือการดัดแปลงโดยผู้ใช้ระบบทดสอบ
หมายเหตุ: ชุดทดสอบ ALEX² รุ่น 02-2001-01 (20 อาร์เรย์) มีไว้สำหรับการประมวลผลด้วยตนเองเท่านั้น หากต้องการใช้ชุดทดสอบ ALEX² รุ่นดังกล่าวกับ MAX 9k อัตโนมัติ จะต้องสั่งซื้อ Washing Solution (REF 00-5003-01) และ Stop Solution (REF 00-5007-01) แยกต่างหาก ข้อมูลผลิตภัณฑ์เพิ่มเติมทั้งหมดสามารถดูได้ในคำแนะนำการใช้งานที่เกี่ยวข้อง: https://www.madx.com/extras.
ชุด ALEX² รุ่น 02-5001-01 (50 อาร์เรย์) สามารถใช้สำหรับการประมวลผลอัตโนมัติด้วยอุปกรณ์ MAX 9k (REF 17-0000-01) เช่นเดียวกับอุปกรณ์ MAX 45k (REF 16-0000-01)
หลักการของกระบวนการ
ALEX² เป็นการทดสอบภูมิคุ้มกันโดยใช้ Enzyme-Linked Immunosorbent Assay (ELISA) สารสกัดสารก่อภูมิแพ้หรือสารก่อภูมิแพ้ระดับโมเลกุลที่จับคู่กับอนุภาคขนาดนาโนจะถูกสะสมในลักษณะเป็นระบบบนเฟสแข็งที่ก่อตัวเป็นอาร์เรย์ระดับมหภาค ขั้นแรก สารก่อภูมิแพ้ที่จับกับอนุภาคจะทำปฏิกิริยากับ IgE เฉพาะที่มีอยู่ในร่างกายของผู้ป่วยampหลังจากฟักตัวแล้ว IgE ที่ไม่จำเพาะจะถูกชะล้างออกไป ขั้นตอนต่อไปคือการเติมแอนติบอดีตรวจจับ IgE ของมนุษย์ที่มีฉลากเอนไซม์ซึ่งจะสร้างสารเชิงซ้อนกับ IgE จำเพาะที่ผูกกับอนุภาค หลังจากขั้นตอนการล้างครั้งที่สอง จะเติมสารตั้งต้นซึ่งจะถูกเปลี่ยนเป็นตะกอนที่มีสีไม่ละลายน้ำโดยเอนไซม์ที่ผูกกับแอนติบอดี ในที่สุด ปฏิกิริยาระหว่างเอนไซม์กับสารตั้งต้นจะหยุดลงโดยการเติมรีเอเจนต์ที่ปิดกั้น ปริมาณของตะกอนจะแปรผันตามความเข้มข้นของ IgE จำเพาะในอุจจาระของผู้ป่วยampขั้นตอนการทดสอบในห้องปฏิบัติการจะตามด้วยการรวบรวมและวิเคราะห์ภาพโดยใช้ระบบแมนนวล (ImageXplorer) หรือระบบอัตโนมัติ (MAX 45k หรือ MAX 9k) ผลการทดสอบจะวิเคราะห์ด้วยซอฟต์แวร์วิเคราะห์ RAPTOR SERVER และรายงานเป็นหน่วยการตอบสนอง IgE (kUA/l) ผล IgE ทั้งหมดจะรายงานเป็นหน่วยการตอบสนอง IgE (kU/l) RAPTOR SERVER มีจำหน่ายในเวอร์ชัน 1 สำหรับหมายเลขเวอร์ชันสี่หลักเต็ม โปรดดูที่เอกสาร RAPTOR SERVER ที่มีให้ที่ www.raptor-server.com/ข้อมูลการพิมพ์.
การจัดส่งและการจัดเก็บ
การจัดส่ง ALEX² จะดำเนินการภายใต้สภาวะอุณหภูมิแวดล้อม อย่างไรก็ตาม ชุดอุปกรณ์จะต้องถูกจัดเก็บทันทีหลังจากจัดส่งที่อุณหภูมิ 2-8°C หากจัดเก็บอย่างถูกต้อง ALEX² และส่วนประกอบต่างๆ จะสามารถใช้งานได้จนถึงวันหมดอายุที่ระบุ
ชุดรีเอเจนต์มีความคงตัวเป็นเวลา 6 เดือนหลังจากเปิด (ในสภาวะการเก็บรักษาที่ระบุ)
การกำจัดขยะ
กำจัดตลับหมึก ALEX² ที่ใช้แล้วและส่วนประกอบของชุดอุปกรณ์ที่ไม่ได้ใช้รวมกับขยะเคมีจากห้องปฏิบัติการ ปฏิบัติตามข้อบังคับทั้งหมดของประเทศ รัฐ และท้องถิ่นเกี่ยวกับการกำจัด
อภิธานศัพท์ของสัญลักษณ์
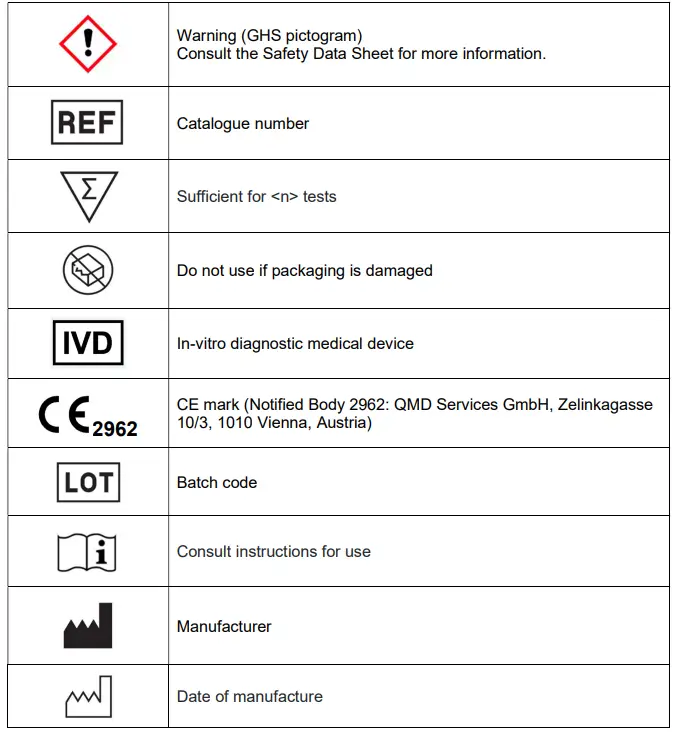
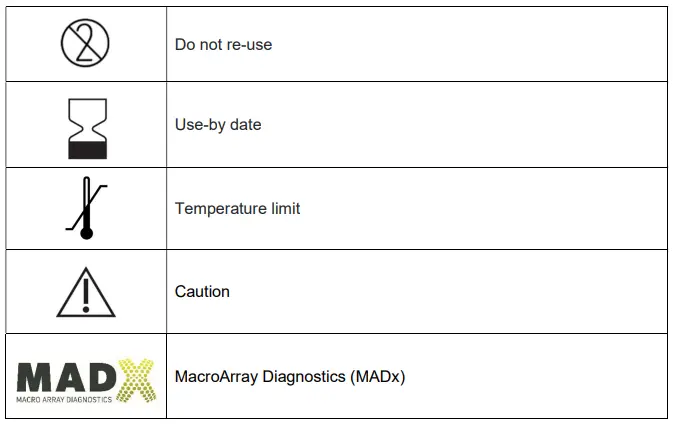
ส่วนประกอบของชุด
ส่วนประกอบแต่ละส่วน (รีเอเจนต์) จะเสถียรจนถึงวันที่ระบุบนฉลากของส่วนประกอบแต่ละส่วน ไม่แนะนำให้รวมรีเอเจนต์จากชุดทดสอบชุดต่างๆ เข้าด้วยกัน หากต้องการดูรายการสารสกัดสารก่อภูมิแพ้และสารก่อภูมิแพ้ระดับโมเลกุลที่ตรึงอยู่ในอาร์เรย์ ALEX² โปรดติดต่อ ฝ่ายสนับสนุน@madx.com.
| ส่วนประกอบชุด REF 02-2001-01 | เนื้อหา | คุณสมบัติ |
| ตลับหมึก ALEX² | 2 ตุ่มน้ำบน ALEX² จำนวน 10 อัน สำหรับการวิเคราะห์ทั้งหมด 20 ครั้ง
การสอบเทียบผ่านมาสเตอร์เคิร์ฟสามารถทำได้ผ่าน RAPTOR SERVER ซอฟต์แวร์วิเคราะห์ |
พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ |
| อเล็กซ์² เอสampเลอเจือจาง | 1 ขวด ขนาด 9 มล. | พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้สารเคมีถึงอุณหภูมิห้องก่อนใช้งาน สารเคมีที่เปิดแล้วมีความคงตัวเป็นเวลา 6 เดือนที่อุณหภูมิ 2-8°C รวมถึงสารยับยั้ง CCD |
| น้ำยาซักผ้า | 2 ขวด ขนาด 50 มล. | พร้อมสำหรับการใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้น้ำยาไปถึงอุณหภูมิห้องก่อนใช้งาน รีเอเจนต์แบบเปิดมีความคงตัวเป็นเวลา 6 เดือนที่ 2-8°C |
| ส่วนประกอบชุด REF 02-2001-01 | เนื้อหา | คุณสมบัติ |
| การตรวจจับแอนติบอดี ALEX² | 1 ขวด ขนาด 11 มล. | พร้อมสำหรับการใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้น้ำยาไปถึงอุณหภูมิห้องก่อนใช้งาน รีเอเจนต์แบบเปิดมีความคงตัวเป็นเวลา 6 เดือนที่ 2-8°C |
| โซลูชันพื้นผิว ALEX² | 1 ขวด ขนาด 11 มล. | พร้อมสำหรับการใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้น้ำยาไปถึงอุณหภูมิห้องก่อนใช้งาน รีเอเจนต์แบบเปิดมีความคงตัวเป็นเวลา 6 เดือนที่ 2-8°C |
| (ALEX²) หยุดการแก้ปัญหา | 1 ขวด ขนาด 2.4 มล. | พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้สารเคมีถึงอุณหภูมิห้องก่อนใช้งาน สารเคมีที่เปิดแล้วมีความคงตัวเป็นเวลา 6 เดือนที่อุณหภูมิ 2-8°C อาจมีลักษณะเป็นสารละลายขุ่นเมื่อเก็บไว้เป็นเวลานาน ซึ่งไม่มีผลต่อผลลัพธ์ |
| ส่วนประกอบชุด REF 02-5001-01 | เนื้อหา | คุณสมบัติ |
| ตลับหมึก ALEX² | 5 ตุ่มน้ำบน ALEX² จำนวน 10 อัน สำหรับการวิเคราะห์ทั้งหมด 50 ครั้ง
การสอบเทียบผ่านกราฟหลักสามารถทำได้ผ่านซอฟต์แวร์วิเคราะห์ RAPTOR SERVER |
พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ |
| อเล็กซ์² เอสampเลอเจือจาง | 1 ขวด ขนาด 30 มล. | พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้สารเคมีถึงอุณหภูมิห้องก่อนใช้งาน สารเคมีที่เปิดแล้วมีความคงตัวเป็นเวลา 6 เดือนที่อุณหภูมิ 2-8°C รวมถึงสารยับยั้ง CCD |
| น้ำยาซักผ้า | 4 x conc. 1 ขวด ขนาด 250 มล. | เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ เจือจาง 1 ถึง 4 ด้วยน้ำที่ผ่านการดีไอออนไนซ์ก่อนใช้งาน ปล่อยให้น้ำยาถึงอุณหภูมิห้องก่อนใช้งาน น้ำยาที่เปิดแล้วมีความคงตัวเป็นเวลา 6 เดือนที่อุณหภูมิ 2-8°C |
| การตรวจจับแอนติบอดี ALEX² | 1 ขวด ขนาด 30 มล. | พร้อมสำหรับการใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้น้ำยาไปถึงอุณหภูมิห้องก่อนใช้งาน รีเอเจนต์แบบเปิดมีความคงตัวเป็นเวลา 6 เดือนที่ 2-8°C |
| ส่วนประกอบชุด REF 02-5001-01 | เนื้อหา | คุณสมบัติ |
| โซลูชันพื้นผิว ALEX² | 1 ขวด ขนาด 30 มล. | พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้น้ำยาถึงอุณหภูมิห้องก่อนใช้งาน น้ำยาที่เปิดแล้วสามารถ
คงตัวได้นาน 6 เดือน ที่อุณหภูมิ 2-8°C |
| (ALEX²) หยุดการแก้ปัญหา | 1 ขวด ขนาด 10 มล. | พร้อมใช้งาน เก็บที่อุณหภูมิ 2-8°C จนถึงวันหมดอายุ ปล่อยให้สารเคมีถึงอุณหภูมิห้องก่อนใช้งาน สารเคมีที่เปิดแล้วมีความคงตัวเป็นเวลา 6 เดือนที่อุณหภูมิ 2-8°C อาจมีลักษณะเป็นสารละลายขุ่นเมื่อเก็บไว้เป็นเวลานาน ซึ่งไม่มีผลต่อผลลัพธ์ |
อุปกรณ์ที่จำเป็นสำหรับการประมวลผลและการวิเคราะห์
การวิเคราะห์ด้วยตนเอง
- ImageXplorer
- Arrayholder (อุปกรณ์เสริม)
- Lab Rocker (มุมเอียง 8° ความเร็วที่ต้องการ 8 rpm)
- ห้องฟักไข่ (กว้างxลึกxสูง – 35x25x2 ซม.)
- ซอฟต์แวร์วิเคราะห์ RAPTOR SERVER
- พีซี/โน๊ตบุ๊ค
อุปกรณ์ที่จำเป็น ไม่ได้จัดเตรียมโดย MADx:
- น้ำที่ผ่านการขจัดแร่ธาตุ
- ปิเปตและทิป (100 µl และ 100 – 1000 µl)
การวิเคราะห์อัตโนมัติ:
- อุปกรณ์ MAX (MAX 45k หรือ MAX 9k)
- น้ำยาซักฟอก (REF 00-5003-01)
- โซลูชั่นหยุด (REF 00-5007-01)
- ซอฟต์แวร์วิเคราะห์ RAPTOR SERVER
- พีซี/โน๊ตบุ๊ค
บริการบำรุงรักษาตามคำแนะนำของผู้ผลิต
การจัดการอาร์เรย์
ห้ามสัมผัสพื้นผิวอาร์เรย์ ข้อบกพร่องบนพื้นผิวที่เกิดจากวัตถุทื่อหรือคมอาจขัดขวางการอ่านผลลัพธ์ที่ถูกต้อง ห้ามถ่ายภาพ ALEX² ก่อนที่อาร์เรย์จะแห้งสนิท (แห้งที่อุณหภูมิห้อง)
คำเตือนและข้อควรระวัง
- ขอแนะนำให้สวมอุปกรณ์ป้องกันมือและตารวมทั้งเสื้อกาวน์แล็บและปฏิบัติตามแนวทางปฏิบัติในห้องปฏิบัติการที่ดีในการเตรียมและจัดการรีเอเจนต์และampเลส.
- เพื่อให้เป็นไปตามแนวปฏิบัติที่ดีในห้องปฏิบัติการ วัสดุที่มาจากมนุษย์ทั้งหมดควรได้รับการพิจารณาว่าอาจติดเชื้อได้ และได้รับการจัดการด้วยความระมัดระวังเช่นเดียวกับผู้ป่วยampเลส.
- อเล็กซ์² เอสampสารเจือจางและสารละลายซักฟอกประกอบด้วยโซเดียมอะไซด์ (<0.1%) เป็นสารกันเสียและต้องจัดการด้วยความระมัดระวัง เอกสารข้อมูลความปลอดภัยมีให้ตามคำขอ
- สารละลายหยุดการทำงาน (ALEX²) ประกอบด้วยสารละลายกรดเอทิลีนไดอะมีนเตตราอะซิติก (EDTA) และต้องใช้ด้วยความระมัดระวัง เอกสารข้อมูลความปลอดภัยมีให้ตามคำขอ
- สำหรับการวินิจฉัยในหลอดทดลองเท่านั้น ห้ามใช้ภายในหรือภายนอกร่างกายในมนุษย์หรือสัตว์
- เฉพาะบุคลากรที่ได้รับการฝึกอบรมในห้องปฏิบัติการเท่านั้นที่ควรใช้ชุดนี้
- เมื่อมาถึง ให้ตรวจสอบส่วนประกอบของชุดว่าได้รับความเสียหายหรือไม่ หากส่วนประกอบใดส่วนหนึ่งได้รับความเสียหาย (เช่น ขวดบัฟเฟอร์) โปรดติดต่อ MADx (ฝ่ายสนับสนุน@madx.com) หรือตัวแทนจำหน่ายในพื้นที่ของคุณ ห้ามใช้ชิ้นส่วนชุดที่ชำรุด เนื่องจากการใช้งานอาจทำให้ชุดทำงานได้อย่างมีประสิทธิภาพน้อยลง
- อย่าใช้รีเอเจนต์เกินวันหมดอายุ
- ห้ามผสมรีเอเจนต์จากแบตช์ที่ต่างกัน
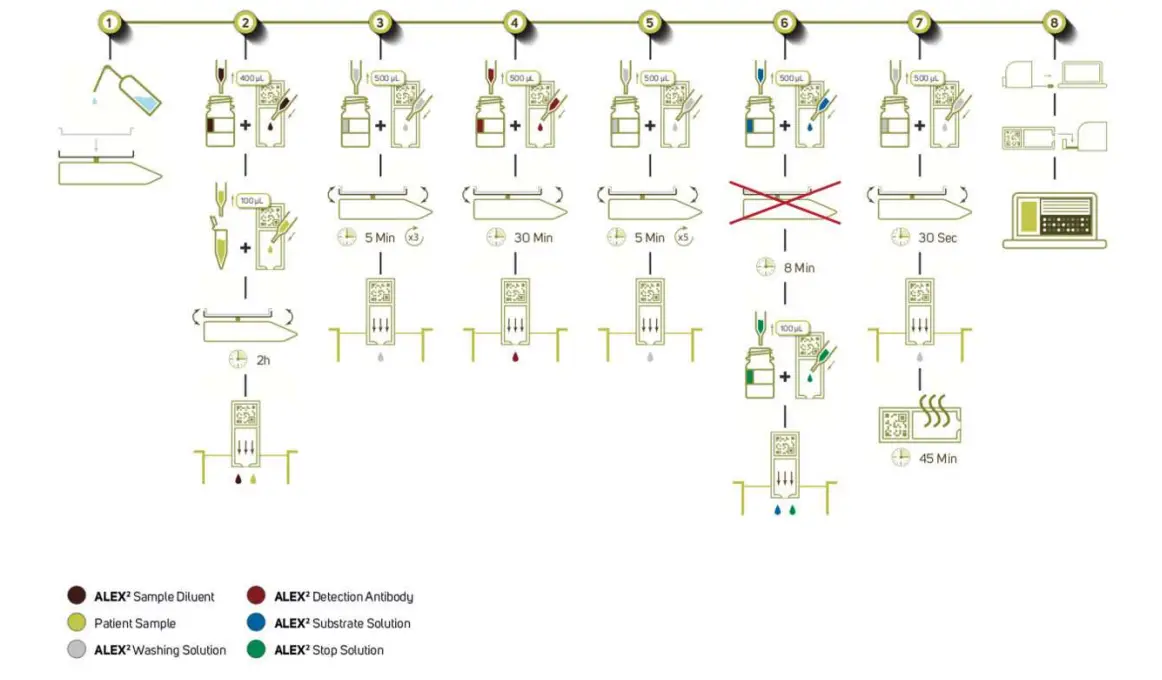
ขั้นตอนการตรวจ ELISA
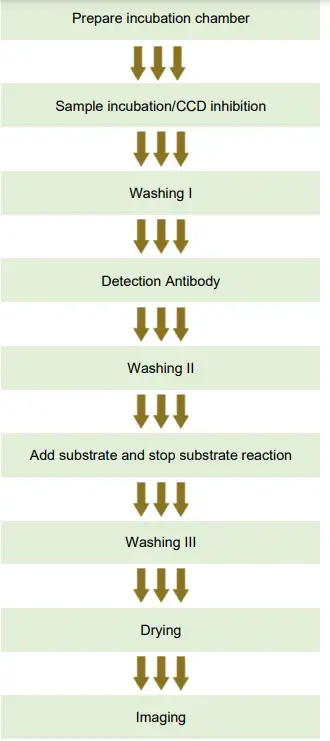
การตระเตรียม
การเตรียม samples: ซีรั่มหรือพลาสมา (เฮปาริน ซิเตรต ไม่มี EDTA)ampสามารถใช้จากเส้นเลือดฝอยหรือเลือดดำได้ เลือด sampไฟล์สามารถรวบรวมได้โดยใช้ขั้นตอนมาตรฐาน ร้านค้า sampที่อุณหภูมิ 2–8°C นานถึงหนึ่งสัปดาห์ เก็บซีรั่มและพลาสมาไว้ampที่อุณหภูมิ -20 องศาเซลเซียส เพื่อการเก็บรักษาเป็นเวลานาน การจัดส่งซีรั่ม/พลาสมา sampที่อุณหภูมิห้องสามารถใช้ได้ อนุญาตเสมอ sampจนถึงอุณหภูมิห้องก่อนใช้งาน
การเตรียมสารละลายสำหรับล้าง (สำหรับ REF 02-5001-01 และ REF 00-5003-01 เมื่อใช้ร่วมกับอุปกรณ์ MAX) เทสารละลายสำหรับล้าง 1 ขวดลงในภาชนะสำหรับล้างของเครื่องมือ เติมน้ำที่ผ่านการดีไอออนไนซ์จนถึงเครื่องหมายสีแดงแล้วค่อยๆ ผสมภาชนะหลายๆ ครั้งโดยไม่ให้เกิดฟอง สารเคมีที่เปิดแล้วจะคงตัวเป็นเวลา 6 เดือนที่อุณหภูมิ 2-8°C
ห้องฟักไข่: ปิดฝาสำหรับขั้นตอนการทดสอบทั้งหมดเพื่อป้องกันความชื้นลดลง
พารามิเตอร์ of ขั้นตอน:
- 100 µl sample + 400 µl ALEX² Sampเลอเจือจาง
- แอนติบอดีตรวจจับ ALEX² ขนาด 500 µl
- สารละลายพื้นผิว ALEX² 500 µl
- สารละลายหยุด 100 µl (ALEX²)
- สารละลายซักล้าง 4500 µl
เวลาทดสอบประมาณ 3 ชั่วโมง 30 นาที (โดยไม่ทำให้อาร์เรย์ที่ประมวลผลแห้ง)
ไม่แนะนำให้ทำการทดสอบเกินกว่าที่สามารถปิเปตได้ภายใน 8 นาที การฟักทั้งหมดดำเนินการที่อุณหภูมิห้อง 20-26°C
สารเคมีทั้งหมดจะต้องใช้ที่อุณหภูมิห้อง (20-26°C) ห้ามทำการทดสอบภายใต้แสงแดดโดยตรง
เตรียมห้องฟักไข่
เปิดห้องฟักและวางกระดาษเช็ดมือไว้ด้านล่าง แช่กระดาษเช็ดมือในน้ำที่ผ่านการดีไอออนไนซ์จนไม่เห็นส่วนที่แห้งของกระดาษเช็ดมือ
Sampการฟักตัว/การยับยั้ง CCD
นำตลับ ALEX² ตามจำนวนที่ต้องการแล้วใส่ลงในช่องใส่ชุดกรอง เติม ALEX² S 400 μlampเติมสารละลายลงในตลับแต่ละตลับ เติมสารละลายสำหรับผู้ป่วย 100 μlampนำไปใส่ในตลับ ให้แน่ใจว่าสารละลายที่ได้กระจายอย่างทั่วถึง วางตลับลงในห้องฟักที่เตรียมไว้ และวางห้องฟักที่มีตลับอยู่บนแท่นโยกห้องทดลอง โดยให้ตลับโยกไปตามด้านยาวของตลับ เริ่มฟักเซรั่มด้วยความเร็ว 8 รอบต่อนาทีเป็นเวลา 2 ชั่วโมง ปิดห้องฟักก่อนเริ่มแท่นโยกห้องทดลอง หลังจากผ่านไป 2 ชั่วโมง ให้ปล่อยสารละลายampลงในภาชนะเก็บสะสม เช็ดหยดน้ำออกจากตลับหมึกอย่างระมัดระวังโดยใช้กระดาษชำระ
หลีกเลี่ยงการสัมผัสพื้นผิวอาร์เรย์ด้วยกระดาษเช็ดมือ! หลีกเลี่ยงการส่งต่อหรือการปนเปื้อนข้ามของ sampระหว่างตลับหมึก ALEX² แต่ละตลับ!
ตัวเลือกหรือ Hom s LF ที่เป็นบวก (เครื่องหมาย CCD): โดยใช้โปรโตคอลการยับยั้งแอนติบอดี CCD มาตรฐาน (ตามที่อธิบายไว้ในวรรค 2:ampการบ่มเพาะ/การยับยั้ง CCD) ประสิทธิภาพการยับยั้ง CCD คือ 85% หากจำเป็นต้องใช้ประสิทธิภาพการยับยั้งในอัตราที่สูงกว่า ให้เตรียมสารละลาย 1 มล.ampหลอดแก้ว เติม ALEX² S 400 μlampสารละลายเจือจางและเซรั่ม 100 μl ฟักเป็นเวลา 30 นาที (ไม่เขย่า) จากนั้นดำเนินการตามขั้นตอนการทดสอบปกติ
บันทึก: ขั้นตอนการยับยั้ง CCD เพิ่มเติมทำให้ในหลายๆ กรณีมีอัตราการยับยั้งแอนติบอดี CCD สูงกว่า 95%
1ก. ซักผ้าฉัน
เติมสารละลายล้าง 500 μl ลงในตลับแต่ละตลับแล้วฟักบนแท่นหมุนห้องทดลอง (ที่ 8 รอบต่อนาที) เป็นเวลา 5 นาที ปล่อยสารละลายล้างลงในภาชนะเก็บและเคาะตลับด้วยกระดาษเช็ดมือแห้งที่วางซ้อนกันอย่างแรง เช็ดหยดที่เหลือออกจากตลับอย่างระมัดระวังโดยใช้กระดาษเช็ดมือ
ทำซ้ำขั้นตอนนี้อีก 2 ครั้ง
เพิ่มการตรวจจับแอนติบอดี
เติม ALEX² Detection Antibody ปริมาณ 500 µl ลงในแต่ละตลับ
ตรวจสอบให้แน่ใจว่าพื้นผิวอาร์เรย์ทั้งหมดถูกคลุมด้วยโซลูชันแอนติบอดีตรวจจับ ALEX²
วางตลับหมึกลงในห้องฟักบนแท่นโยกแล็บ แล้วฟักที่ความเร็ว 8 รอบต่อนาทีเป็นเวลา 30 นาที ปล่อยสารละลายแอนติบอดีตรวจจับลงในภาชนะเก็บตัวอย่าง แล้วเคาะตลับหมึกกับกระดาษเช็ดมือแห้งที่วางซ้อนกันอย่างแรง เช็ดหยดที่เหลือออกจากตลับหมึกอย่างระมัดระวังโดยใช้กระดาษเช็ดมือ
2ก. ซักผ้าII
เติมสารละลายล้าง 500 μl ลงในตลับแต่ละตลับแล้วฟักบนแท่นหมุนทดลองที่ความเร็ว 8 รอบต่อนาทีเป็นเวลา 5 นาที ปล่อยสารละลายล้างลงในภาชนะเก็บและเคาะตลับด้วยกระดาษเช็ดมือแห้งที่วางซ้อนกันอย่างแรง เช็ดหยดที่เหลือออกจากตลับอย่างระมัดระวังโดยใช้กระดาษเช็ดมือ
ทำซ้ำขั้นตอนนี้อีก 4 ครั้ง
3+4. เติมสารละลายพื้นผิว ALEX² และหยุดปฏิกิริยาของพื้นผิว
เติมสารละลายซับสเตรต ALEX² 500 μl ลงในตลับแต่ละตลับ เริ่มจับเวลาด้วยการเติมตลับแรกและดำเนินการเติมตลับที่เหลือ ตรวจสอบให้แน่ใจว่าพื้นผิวของอาร์เรย์ทั้งหมดถูกปกคลุมด้วยสารละลายซับสเตรต และฟักอาร์เรย์เป็นเวลา 8 นาทีพอดีโดยไม่ต้องเขย่า (เขย่าห้องทดลองที่ 0 รอบต่อนาทีและในตำแหน่งแนวนอน)
หลังจากผ่านไป 8 นาทีพอดี ให้เติมสารละลายหยุดการตกตะกอน (ALEX²) 100 μl ลงในตลับทั้งหมด โดยเริ่มจากตลับแรกเพื่อให้แน่ใจว่ามีการฟักสารละลายซับสเตรต ALEX² ในทุกชุดเป็นเวลาเท่ากัน เขย่าเบาๆ เพื่อให้สารละลายหยุดการตกตะกอน (ALEX²) กระจายอย่างทั่วถึงในตลับทั้งหมด หลังจากปิเปตสารละลายหยุดการตกตะกอน (ALEX²) ลงบนทุกชุด จากนั้นเทสารละลายซับสเตรต/สารละลายหยุดการตกตะกอน (ALEX²) ออกจากตลับ แล้วเคาะตลับด้วยกระดาษเช็ดมือแห้งที่วางซ้อนกันอย่างแรง เช็ดหยดที่เหลือออกจากตลับอย่างระมัดระวังโดยใช้กระดาษเช็ดมือ
Lab Rocker จะต้องไม่สั่นในระหว่างการฟักตัวของวัสดุพิมพ์!
4ก. ซักผ้า III
เติมสารละลายล้าง 500 μl ลงในตลับแต่ละตลับแล้วฟักบนแท่นหมุนทดลองที่ความเร็ว 8 รอบต่อนาทีเป็นเวลา 30 วินาที ปล่อยสารละลายล้างลงในภาชนะเก็บและเคาะตลับด้วยกระดาษเช็ดมือแห้งที่วางซ้อนกันอย่างแรง เช็ดหยดที่เหลือออกจากตลับอย่างระมัดระวังโดยใช้กระดาษเช็ดมือ
การวิเคราะห์ภาพ
หลังจากเสร็จสิ้นขั้นตอนการทดสอบแล้ว ให้ปล่อยให้แห้งในอากาศที่อุณหภูมิห้องจนกว่าจะแห้งสนิท (อาจใช้เวลานานถึง 45 นาที)
การทำให้แห้งสนิทเป็นสิ่งสำคัญสำหรับความไวของการทดสอบ เฉพาะอาร์เรย์ที่แห้งสนิทเท่านั้นที่ให้อัตราส่วนสัญญาณต่อสัญญาณรบกวนที่เหมาะสม
ในที่สุดอาร์เรย์ที่แห้งแล้วจะถูกสแกนด้วย ImageXplorer หรืออุปกรณ์ MAX และวิเคราะห์ด้วยซอฟต์แวร์ RAPTOR SERVER Analysis (ดูรายละเอียดในคู่มือซอฟต์แวร์ RAPTOR SERVER) ซอฟต์แวร์ RAPTOR SERVER Analysis จะได้รับการตรวจยืนยันร่วมกับเครื่องมือ ImageXplorer และอุปกรณ์ MAX เท่านั้น ดังนั้น MADx จึงไม่รับผิดชอบต่อผลลัพธ์ใดๆ ที่ได้รับจากอุปกรณ์จับภาพอื่นๆ (เช่น สแกนเนอร์)
การสอบเทียบชุดทดสอบ
เส้นโค้งการสอบเทียบหลัก ALEX² ถูกสร้างขึ้นโดยการทดสอบอ้างอิงกับการเตรียมซีรั่มที่มี IgE เฉพาะกับแอนติเจนต่างๆ ที่ครอบคลุมช่วงการวัดที่ต้องการ พารามิเตอร์การสอบเทียบเฉพาะล็อตนั้นจัดทำโดยซอฟต์แวร์การวิเคราะห์ RAPTOR SERVER ผลการทดสอบ sIgE ของ ALEX² แสดงเป็น kUA/l ผล IgE ทั้งหมดเป็นแบบกึ่งเชิงปริมาณและคำนวณจากการวัด anti-IgE ด้วยปัจจัยการสอบเทียบเฉพาะล็อต ซึ่งจัดทำโดยซอฟต์แวร์การวิเคราะห์ RAPTOR SERVER และเลือกตามรหัส QR เฉพาะล็อต
พารามิเตอร์เส้นโค้งสำหรับแต่ละล็อตได้รับการปรับโดยระบบทดสอบอ้างอิงภายในองค์กร โดยเปรียบเทียบกับการเตรียมซีรั่มที่ทดสอบบน ImmunoCAP (Thermo Fisher Scientific) สำหรับ IgE เฉพาะกับสารก่อภูมิแพ้หลายชนิด ดังนั้น ผลลัพธ์ ALEX² จึงสามารถตรวจสอบย้อนกลับโดยอ้อมกับการเตรียมอ้างอิง WHO 11/234 สำหรับ IgE ทั้งหมด
ความแปรผันอย่างเป็นระบบในระดับสัญญาณระหว่างล็อตจะได้รับการทำให้เป็นมาตรฐานโดยการสอบเทียบแบบต่างสายพันธุ์กับเส้นโค้งอ้างอิง IgE ปัจจัยการแก้ไขจะถูกใช้เพื่อปรับค่าเบี่ยงเบนการวัดเฉพาะล็อตอย่างเป็นระบบ
ช่วงการวัด
IgE จำเพาะ: 0.3-50 kUA/l เชิงปริมาณ
IgE ทั้งหมด: 20-2500 kU/l กึ่งเชิงปริมาณ
การควบคุมคุณภาพ
การเก็บบันทึกสำหรับการทดสอบแต่ละครั้ง
ตามหลักปฏิบัติที่ดีของห้องปฏิบัติการ ขอแนะนำให้บันทึกหมายเลขล็อตของสารเคมีทั้งหมดที่ใช้
ตัวอย่างการควบคุม
ตามแนวทางปฏิบัติที่ดีในห้องปฏิบัติการ แนะนำให้มีการควบคุมคุณภาพamples จะรวมอยู่ในช่วงที่กำหนด ค่าอ้างอิงสำหรับซีรั่มควบคุมที่มีจำหน่ายในเชิงพาณิชย์บางตัวสามารถให้โดย MADx ได้ตามคำขอ
การวิเคราะห์ข้อมูล
สำหรับการวิเคราะห์ภาพของอาร์เรย์ที่ประมวลผลแล้ว ต้องใช้ ImageXplorer หรืออุปกรณ์ MAX ภาพ ALEX² จะถูกวิเคราะห์โดยอัตโนมัติโดยใช้ซอฟต์แวร์วิเคราะห์ RAPTOR SERVER และจะสร้างรายงานสรุปผลลัพธ์สำหรับผู้ใช้
ผลลัพธ์
ALEX² คือการทดสอบ ELISA เชิงปริมาณสำหรับ IgE เฉพาะและวิธีกึ่งเชิงปริมาณสำหรับ IgE ทั้งหมด แอนติบอดี IgE เฉพาะต่อสารก่อภูมิแพ้จะแสดงเป็นหน่วยการตอบสนอง IgE (kUA/l) โดยผล IgE ทั้งหมดจะแสดงเป็น kU/l ซอฟต์แวร์วิเคราะห์ RAPTOR SERVER จะคำนวณและรายงานผล sIgE (เชิงปริมาณ) และผล tIgE (เชิงปริมาณ) โดยอัตโนมัติ
ข้อจำกัดของขั้นตอน
การวินิจฉัยทางคลินิกที่ชัดเจนควรทำร่วมกับผลการตรวจทางคลินิกที่มีอยู่ทั้งหมดโดยผู้เชี่ยวชาญทางการแพทย์เท่านั้น และไม่ควรอิงจากผลการวินิจฉัยวิธีเดียวเท่านั้น
ในพื้นที่การประยุกต์ใช้บางพื้นที่ (เช่น การแพ้อาหาร) แอนติบอดี IgE ที่หมุนเวียนอาจยังคงตรวจไม่พบแม้ว่าอาการทางคลินิกของการแพ้อาหารต่อสารก่อภูมิแพ้บางชนิดอาจเกิดขึ้นก็ตาม เนื่องจากแอนติบอดีเหล่านี้อาจจำเพาะกับสารก่อภูมิแพ้ที่ถูกปรับเปลี่ยนระหว่างการแปรรูปทางอุตสาหกรรม การปรุงอาหาร หรือการย่อย และด้วยเหตุนี้จึงไม่มีอยู่ในอาหารเดิมที่ใช้ทดสอบผู้ป่วย
ผลพิษที่เป็นลบบ่งชี้ถึงระดับแอนติบอดี IgE ที่จำเพาะต่อพิษที่ตรวจไม่พบ (เช่น จากการไม่สัมผัสเป็นเวลานาน) และไม่ตัดความเป็นไปได้ของการมีอาการแพ้พิษแมลงต่อยทางคลินิก
ในเด็ก โดยเฉพาะอายุต่ำกว่า 2 ปี ช่วงปกติของ tIgE จะต่ำกว่าในวัยรุ่นและผู้ใหญ่ [7] ดังนั้น จึงคาดว่าในเด็กอายุน้อยกว่า 2 ปีในสัดส่วนที่สูงกว่า ระดับ IgE รวมจะต่ำกว่าขีดจำกัดการตรวจจับที่กำหนด ข้อจำกัดนี้ใช้ไม่ได้กับการวัด IgE ที่เฉพาะเจาะจง
ค่าที่คาดหวัง
ความสัมพันธ์อย่างใกล้ชิดระหว่างระดับแอนติบอดี IgE เฉพาะต่อสารก่อภูมิแพ้และโรคภูมิแพ้เป็นที่ทราบกันดีและมีการอธิบายไว้อย่างละเอียดในเอกสาร [1] ผู้ป่วยแต่ละรายที่ไวต่อสารก่อภูมิแพ้จะแสดงระดับ IgE เฉพาะบุคคลfile เมื่อทดสอบด้วย ALEX² การตอบสนองของ IgE ด้วย sampเลซจากบุคคลที่ไม่มีอาการแพ้และมีสุขภาพแข็งแรงจะมีค่าต่ำกว่า 0.3 kUA/l สำหรับสารก่อภูมิแพ้โมเลกุลเดี่ยวและสำหรับสารสกัดสารก่อภูมิแพ้เมื่อทดสอบด้วย ALEX² พื้นที่อ้างอิงสำหรับ IgE ทั้งหมดในผู้ใหญ่คือ < 100 kU/l แนวทางปฏิบัติที่ดีของห้องปฏิบัติการแนะนำให้ห้องปฏิบัติการแต่ละแห่งกำหนดค่าที่คาดหวังของตนเอง
ลักษณะการทำงาน
ลักษณะการทำงานรวมถึงสรุปความปลอดภัยและประสิทธิภาพสามารถพบได้ใน MADx webเว็บไซต์: https://www.madx.com/extras.
การรับประกัน
ข้อมูลประสิทธิภาพการทำงานได้รับโดยใช้ขั้นตอนที่ระบุไว้ในคำแนะนำการใช้งานนี้ การเปลี่ยนแปลงหรือแก้ไขขั้นตอนใดๆ อาจส่งผลต่อผลลัพธ์ และ MacroArray Diagnostics ปฏิเสธการรับประกันใดๆ ที่ระบุ (รวมถึงการรับประกันโดยนัยของความสามารถในการขายและความเหมาะสมในการใช้งาน) ในกรณีดังกล่าว ดังนั้น MacroArray Diagnostics และผู้จัดจำหน่ายในพื้นที่จึงจะไม่รับผิดชอบต่อความเสียหายทางอ้อมหรือเป็นผลสืบเนื่องในกรณีดังกล่าว
คำย่อ
| อเล็กซ์ | อัลเทอรีคเอ็กซ์พลอเรอร์ |
| ซีซีดี | ตัวกำหนดคาร์โบไฮเดรตแบบไขว้ |
| อีดีทีเอ | กรดเอทิลีนไดอะมีนเตตราอะซิติก |
| เอลิซ่า | การวิเคราะห์การดูดซับภูมิคุ้มกันด้วยเอนไซม์เชื่อมโยง |
| อิจีอี | อิมมูโนโกลบูลินอี |
| IVD | การวินิจฉัยในหลอดทดลอง |
| กิโล/ลิตร | หน่วยกิโลกรัมต่อลิตร |
| กว้า/ล | หน่วยกิโลกรัมของ IgE เฉพาะสารก่อภูมิแพ้ต่อลิตร |
| แมดเอ็กซ์ | การวินิจฉัย MacroArray |
| อ้างอิง | หมายเลขอ้างอิง |
| รอบต่อนาที | รอบต่อนาที |
| ซิกอี | IgE เฉพาะสารก่อภูมิแพ้ |
| เวลา | อิกอีรวม |
| ไมโคร | ไมโครลิตร |
รายชื่อสารก่อภูมิแพ้ ALEX²
สารสกัดสารก่อภูมิแพ้: Aca m, Aca s, Ach d, Ail a, All c, All s, Ama r, Amb a, Ana o, Api m, Art v, Ave s, Ber e, Bos d meat, Bos d milk, Bro p, Cam d, Can f ♂ ปัสสาวะ, Can s, Cap a, Cap h epithelia, Cap h milk, Car c, Car i, Car p, Che a, Che q, Chi spp., Cic a, Cit s, Cla h, Clu h, Cor a pollen, Cuc p, Cup s, Cyn d, Dau c, Dol spp., Equ c milk, Equ c meat, Fag e, Fic b, Fic c, Fra e, Gad m, Gal d meat, Gal d white, Gal d yolk, Hel a, Hom g, Hor v, Jug r, Jun a, Len c, Lit s, Loc m, Lol spp., Lup a, Mac i, Man i, Mel g, Mor r, Mus a, Myt e, Ori v, Ory meat, Ory s, Ost e, Ovi a epithelia, Ovi a meat, Ovi a milk, Pan b, Pan m, Pap s, Par j, Pas n, Pec spp., Pen ch, Per a, Pers a, Pet c, Pha v, Phr c, Pim a, Pis s, Pla, Pol d, Pop n, Pru av, Pru du, Pyr c, Raj c, Rat n, Rud spp., Sac c, Sal k, Sal s, Sco s, Sec c dough, Sec c pollen, Ses i, Sin, Sol spp., Sola l, Sol t, Sus d epithel, Sus d meat, Ten m, Thu a, Tri fo, Tri s, Tyr p, Ulm c, Urt d, แวคม, เวสว, แป้งซีแอม
ส่วนประกอบธรรมชาติที่บริสุทธิ์: nAct d 1, nApi m 1, nAra h 1, nAra h 3, nBos d 4, nBos d 5, nBos d 6, nBos d 8, nCan f 3, nCor a 9, nCor a 11, nCup a 1, nCry j 1, nEqu c 3, nFag e 2, nGad m 1, nGad m 2 + 3, nGal d 2, nGal d 3, nGal d 4, nGal d 5, nGly m 5, nGly m 6, nJug r 4, nMac i 2S อัลบูมิน, nOle e 7 (RUO), nPap s 2S อัลบูมิน, nPis v 3, nPla ก 2, nTri ก aA_TI
ส่วนประกอบรีคอมบิแนนท์: rAct d 10, rAct d 2, rAct d 5, rAln g 1, rAln g 4, rAlt a 1, rAlt a 6, rAmb a 1, rAmb a 4, rAna o 2, rAna o 3, rAni s 1, rAni s 3, rApi g 1, rApi g 2, rApi g 6, rApi m 10, rAra h 2, rAra h 6, rAra h 8, rAra h 9, rAra h 15, rArg r 1, rArt v 1, rArt v 3, rAsp f 1, rAsp f 3, rAsp f 4, rAsp f 6, rBer e 1, rBet v 1, rBet v 2, rBet v 6, rBla g 1, rBla g 2, rBla g 4, rBla g 5, rBla g 9, rBlo t 10, rBlo t 21, rBlo t 5, rBos d 2, rCan f 1, rCan f 2, rCan f 4, rCan f 6, rCan f Fel d 1 เช่น, rCan s 3, rCav p 1, rChe a 1, rCla h 8, rClu h 1, rCor a 1.0103, rCor a 1.0401, rCor a 8, rCor a 12 (RUO), rCor a 14, rCra c 6, , rCuc m 2, rCyn d 1, rCyp c 1, rDau c 1, rDer f 1, rDer f 2, rDer p 1, rDer p 10, rDer p 11, rDer p 2, rDer p 20, rDer p 21, rDer p 23, rDer p 5, rDer p 7, rEqu c 1, rEqu c 4, rFag s 1, rFel d 1, rFel d 2, rFel d 4, rFel d 7, rFra a 1 + 3, rFra e 1, rGal d 1, rGly d 2, rGly m 4, rGly m 8, rHev b 1, rHev b 3, rHev b 5, rJug r 6.02, rJug r 8, rLep d 11, rLol p 1, rMal 2, rMal d 3, rMala s 6, rMala s 2, rMala s 1, rMal d 1, rMer a 3, rMes a 11 (RUO), rMus m 5, rOle e 6, rOle e 2, rOry c 1, rOry c 1, rOry c 1, rPar j 1, rPen m 9, rPen m 1, rPen m 2, rPhl p 3, rPhl p 2, rPhl p 1, rPhl p 2, rPhl p 3, rPhl p 4, rPhl p 7, rPho d 1, rPhod s 12, rPis v rPis v 2, rPis v 5.0101 (RUO), rPla a 6, rPla a 7, rPla l 2, rPol d 1, rPru p 1, rPru p 2 (RUO), rRaj c Parvalbumin, rSal k 4, rSal s 1, rSco s 3, rSes i 1, rSin 5, rSola l 3, rSus d 7, rThu a 1, rTri a 1, rTri a 1, rTyr p 1, rVes v 1, rVes v 6, rVit v 1, rXip g 1, rZea m 14
เอกสารอ้างอิง
- แฮมิลตัน, RG. (2008). การประเมินโรคภูมิแพ้ในมนุษย์. ภูมิคุ้มกันวิทยาคลินิก. 1471-1484. 10.1016/B978-0-323-04404-2.10100-9.
- Harwanegg C, Laffer S, Hiller R, Mueller MW, Kraft D, Spitzauer S, Valenta R. สารก่อภูมิแพ้รีคอมบิแนนท์ที่ผ่านการไมโครอาร์เรย์เพื่อการวินิจฉัยโรคภูมิแพ้ Clin Exp Allergy. 2003 Jan;33(1):7-13. doi: 10.1046/j.1365-2222.2003.01550.x. PMID: 12534543
- ฮิลเลอร์ อาร์, ลาฟเฟอร์ เอส, ฮาร์วาเน็กก์ ซี, ฮูเบอร์ เอ็ม, ชมิดท์ ดับเบิลยูเอ็ม, ทวาร์ดอสซ์ เอ, บาร์เล็ตต้า บี, เบ็คเกอร์ ดับเบิลยูเอ็ม, บลาเซอร์ เค, ไบรเทนเดอร์ เอช, แชปแมน เอ็ม, คราเมรี่ อาร์, ดูเชน เอ็ม, เฟอร์ไรรา เอฟ, ฟีบิก เอช, ฮอฟฟ์มันน์-ซอมเมอร์กรูเบอร์ เค, คิง ทีพี, เคลเบอร์-แยงเก้ ที, คูรุป รองประธาน, เลห์เรอร์ เอสบี, ลิดโฮล์ม เจ, มุลเลอร์ ยู, พีนี่ ซี, รีส จี, ไชเนอร์ โอ, เชย์เนียส เอ, เชน เอชดี, สปิทเซาเออร์ เอส, ซัค อาร์, สโวโบดา ไอ, โธมัส ดับเบิลยู, ติงกีโน อาร์, Van Hage-Hamsten M, Virtanen T, Kraft D, Müller MW, Valenta R. โมเลกุลของสารก่อภูมิแพ้แบบ Microarrayed: ผู้เฝ้าประตูวินิจฉัยสำหรับการรักษาโรคภูมิแพ้ FASEB J. 2002 มี.ค.;16(3):414-6. doi: 10.1096/fj.01-0711fje. Epub 2002 ม.ค. 14. PMID: 11790727
- Ferrer M, Sanz ML, Sastre J, Bartra J, del Cuvillo A, Montoro J, Jáuregui I, Dávila I, Mullol J, Valero A. การวินิจฉัยทางโมเลกุลในวิชาภูมิแพ้: การประยุกต์ใช้เทคนิคไมโครอาร์เรย์ J Investig Allergol Clin Immunol. 2009;19 Suppl 1:19-24. PMID: 19476050
- Ott H, Fölster-Holst R, Merk HF, Baron JM. ไมโครอาร์เรย์สารก่อภูมิแพ้: เครื่องมือใหม่สำหรับการสร้างโปรไฟล์ IgE ที่มีความละเอียดสูงในผู้ใหญ่ที่มีโรคผิวหนังอักเสบจากภูมิแพ้ Eur J Dermatol. 2010 ม.ค.-ก.พ.;20(1):54-
61. ดอย: 10.1684/ejd.2010.0810. Epub 2009 2 ต.ค. PMID: 19801343 - Sastre J. การวินิจฉัยระดับโมเลกุลในโรคภูมิแพ้ Clin Exp Allergy. 2010 ต.ค.;40(10):1442-60. doi: 10.1111/j.1365-2222.2010.03585.x. Epub 2010 ส.ค. 2 PMID: 20682003
- Martins TB, Bandhauer ME, Bunker AM, Roberts WL, Hill HR ช่วงเวลาอ้างอิงใหม่สำหรับ IgE รวมในวัยเด็กและผู้ใหญ่ J Allergy Clin Immunol กุมภาพันธ์ 2014;133(2):589-91
สำหรับรายละเอียดเกี่ยวกับการศึกษาวิเคราะห์และทางคลินิกที่ดำเนินการ โปรดดูลักษณะการทำงานที่ https://www.madx.com/extras.
ประวัติการเปลี่ยนแปลง
| เวอร์ชัน | คำอธิบาย | แทนที่ |
| 11 | nGal d1 เปลี่ยนเป็น rGal d1; URL อัพเดทเป็น madx.com; CE เสริมด้วยหมายเลขของหน่วยงานที่แจ้ง; เพิ่มประวัติการเปลี่ยนแปลง | 10 |

© ลิขสิทธิ์โดย MacroArray Diagnostics
การวินิจฉัย MacroArray (MADx)
เล็มบ็อคกาสเซ่ 59 ท็อป 4
1230 เวียนนา ออสเตรีย
+43 (0)1 865 2573
www.madx.com
หมายเลขเวอร์ชัน: 02-IFU-01-EN-11 เปิดตัว: 09-2024
คู่มือแนะนำ
การวินิจฉัย MacroArray
เล็มบ็อคกาสเซ่ 59 ท็อป 4
1230 เวียนนา
madx.com
ซีอาร์เอ็น 448974 ก
เอกสาร / แหล่งข้อมูล
 |
MacroArray ALLERGY XPLORER การวินิจฉัยมาโครอาร์เรย์ [พีดีเอฟ] คำแนะนำ 91201229202JQ, 02-2001-01, 02-5001-01, ALLERGY XPLORER Macro Array Diagnostics, ALLERGY XPLORER, การวินิจฉัย Macro Array, การวินิจฉัย Array, การวินิจฉัย |




