MacroArray ALLERGY XPLORER Makro-Array-Diagnostik
Technische Daten
- Produktname: Grundlegende UDI-DI 91201229202JQ
- Referenznummern: REF 02-2001-01, 02-5001-01
- Verwendungszweck: Nachweis von allergenspezifischem IgE (sIgE) quantitativ und Gesamt-IgE (tIgE) semiquantitativ
- Anwender: Geschultes Laborpersonal und medizinisches Fachpersonal in einem medizinischen Labor
- Lagerung: Die Reagenzien des Kits sind nach dem Öffnen 6 Monate lang stabil
Anweisungen zur Produktverwendung
Verfahrensprinzip
Das Produkt weist allergenspezifisches IgE quantitativ und Gesamt-IgE semiquantitativ nach.
Versand und Lagerung
Stellen Sie sicher, dass die Kit-Reagenzien wie angegeben gelagert und innerhalb von 6 Monaten nach dem Öffnen verwendet werden.
Abfallentsorgung:
Befolgen Sie die Vorschriften zur ordnungsgemäßen Abfallentsorgung.
Kit-Komponenten
Detaillierte Informationen zu den Kitkomponenten finden Sie im Benutzerhandbuch.
Erforderliche Ausrüstung
Manuelle Analyse: Stellen Sie sicher, dass Sie über die vom Hersteller bereitgestellte erforderliche Ausrüstung verfügen.
Automatische Analyse: Verwenden Sie das MAX-Gerät, die Waschlösung, die Stopplösung, die RAPTOR SERVER-Analysesoftware und einen PC/Laptop. Befolgen Sie die Wartungsanweisungen sorgfältig.
Handhabung von Arrays
Befolgen Sie die Anweisungen zum Umgang mit Arrays sorgfältig, um genaue Ergebnisse zu gewährleisten.
Warnhinweise und Vorsichtsmaßnahmen
- Tragen Sie geeignete Schutzausrüstung wie Hand- und Augenschutz und Laborkittel.
- Umgang mit Reagenzien und samples gemäß guter Laborpraxis.
- Behandeln Sie sämtliche Materialien menschlichen Ursprungs als potenziell infektiös und gehen Sie vorsichtig damit um.
Häufig gestellte Fragen
- F: Wie lange sind die Kit-Reagenzien stabil?
A: Die Kit-Reagenzien sind nach dem Öffnen 6 Monate lang stabil, wenn sie unter den angegebenen Bedingungen gelagert werden. - F: Wer kann dieses Produkt verwenden?
A: Dieses Produkt ist für die Verwendung durch geschultes Laborpersonal und medizinisches Fachpersonal in medizinischen Laborumgebungen vorgesehen.
www.madx.com
ALLERGY XPLORER (ALEX²) GEBRAUCHSANWEISUNG
BESCHREIBUNG
Der Allergy Xplorer (ALEX²) ist ein auf einem Enzyme-Linked Immunosorbent Assay (ELISA) basierender In-vitro-Diagnosetest zur quantitativen Messung von allergenspezifischem IgE (sIgE).
Diese Gebrauchsanweisung ist für folgende Produkte gültig:
| Grundlegende UDI-DI | Referenz | Produkt |
| 91201229202JQ | 02-2001-01 | ALEX² für 20 Analysen |
| 02-5001-01 | ALEX² für 50 Analysen |
VERWENDUNGSZWECK
Der ALEX² Allergy Xplorer ist ein Testkit zur In-vitro-Untersuchung von menschlichem Serum oder Plasma (Ausnahme EDTA-Plasma), das in Verbindung mit anderen klinischen Befunden oder diagnostischen Testergebnissen Informationen zur Unterstützung der Diagnose von Patienten mit IgE-vermittelten Erkrankungen liefert.
Das IVD-Medizinprodukt weist allergenspezifisches IgE (sIgE) quantitativ und Gesamt-IgE (tIgE) semiquantitativ nach. Das Produkt wird von geschultem Laborpersonal und medizinischem Fachpersonal in einem medizinischen Labor verwendet.
ZUSAMMENFASSUNG UND ERKLÄRUNG DES TESTS
Allergische Reaktionen sind sofortige Überempfindlichkeitsreaktionen vom Typ I und werden durch Antikörper der Immunglobulinklasse IgE vermittelt. Nach Kontakt mit bestimmten Allergenen führt die IgE-vermittelte Freisetzung von Histamin und anderen Mediatoren aus Mastzellen und Basophilen zu klinischen Manifestationen wie Asthma, allergischer Rhinokonjunktivitis, atopischem Ekzem und gastrointestinalen Symptomen [1]. Daher hilft ein detailliertes Sensibilisierungsmuster gegenüber bestimmten Allergenen bei der Beurteilung von allergischen Patienten [2-6]. Es gibt keine Einschränkung hinsichtlich der Testpopulation. Bei der Entwicklung von IgE-Tests werden Alter und Geschlecht normalerweise nicht als kritische Faktoren berücksichtigt, da die in diesen Tests gemessenen IgE-Werte je nach demografischen Merkmalen nicht signifikant variieren.
Alle wichtigen Allergenquellen des Typs I werden von ALEX² abgedeckt. Eine vollständige Liste der ALEX²-Allergenextrakte und molekularen Allergene finden Sie am Ende dieser Anleitung.
Wichtige Information für den Benutzer!
Für den korrekten Einsatz von ALEX² ist es erforderlich, dass der Anwender diese Gebrauchsanweisung sorgfältig liest und befolgt. Für eine Verwendung dieses Testsystems, die nicht in diesem Dokument beschrieben ist, oder für vom Anwender vorgenommene Änderungen am Testsystem übernimmt der Hersteller keine Haftung.
Achtung: Die Kitvariante 02-2001-01 des ALEX²-Tests (20 Arrays) ist ausschließlich für die manuelle Abarbeitung vorgesehen. Für die Verwendung dieser ALEX²-Kitvariante mit dem automatisierten MAX 9k müssen die Waschlösung (REF 00-5003-01) und die Stopplösung (REF 00-5007-01) separat bestellt werden. Alle weiteren Produktinformationen finden Sie in der entsprechenden Gebrauchsanweisung: https://www.madx.com/extras.
Die ALEX² Kitvariante 02-5001-01 (50 Arrays) kann zur automatisierten Verarbeitung mit dem MAX 9k (REF 17-0000-01) sowie dem MAX 45k (REF 16-0000-01) Gerät verwendet werden.
PRINZIP DES VERFAHRENS
ALEX² ist ein Immunoassay-Test, der auf einem Enzyme-Linked Immunosorbent Assay (ELISA) basiert. Allergenextrakte oder molekulare Allergene, die an Nanopartikel gekoppelt sind, werden systematisch auf einer festen Phase abgelagert und bilden eine makroskopische Anordnung. Zunächst reagieren die partikelgebundenen Allergene mit spezifischem IgE, das im Körper des Patienten vorhanden ist.ampNach der Inkubation wird unspezifisches IgE abgewaschen. Anschließend wird ein enzymmarkierter Anti-Human-IgE-Nachweisantikörper zugegeben, der mit dem partikelgebundenen spezifischen IgE einen Komplex bildet. Nach einem zweiten Waschschritt wird Substrat zugegeben, das durch das antikörpergebundene Enzym in einen unlöslichen, gefärbten Niederschlag umgewandelt wird. Schließlich wird die Enzym-Substrat-Reaktion durch Zugabe eines Blockierungsreagenzes gestoppt. Die Niederschlagsmenge ist proportional zur Konzentration des spezifischen IgE im Patientenkörper.ample. Auf das Labortestverfahren folgt die Bildaufnahme und -analyse entweder mit dem manuellen System (ImageXplorer) oder dem automatisierten System (MAX 45k oder MAX 9k). Die Testergebnisse werden mit der RAPTOR SERVER-Analysesoftware analysiert und in IgE-Reaktionseinheiten (kUA/l) angegeben. Die Gesamt-IgE-Ergebnisse werden ebenfalls in IgE-Reaktionseinheiten (kU/l) angegeben. RAPTOR SERVER ist in Version 1 erhältlich. Die vollständige vierstellige Versionsnummer finden Sie im RAPTOR SERVER-Impressum unter www.raptor-server.com/impressum.
VERSAND UND LAGERUNG
Der Versand von ALEX² erfolgt bei Raumtemperatur. Dennoch muss das Kit sofort nach Erhalt bei 2-8°C gelagert werden. Bei richtiger Lagerung sind ALEX² und seine Komponenten bis zum angegebenen Verfallsdatum verwendbar.
Kit-Reagenzien sind nach dem Öffnen 6 Monate haltbar (bei den angegebenen Lagerbedingungen).
MÜLLENTSORGUNG
Entsorgen Sie die gebrauchte ALEX²-Kartusche und unbenutzte Kitkomponenten mit dem chemischen Laborabfall. Beachten Sie alle nationalen, staatlichen und örtlichen Vorschriften zur Entsorgung.
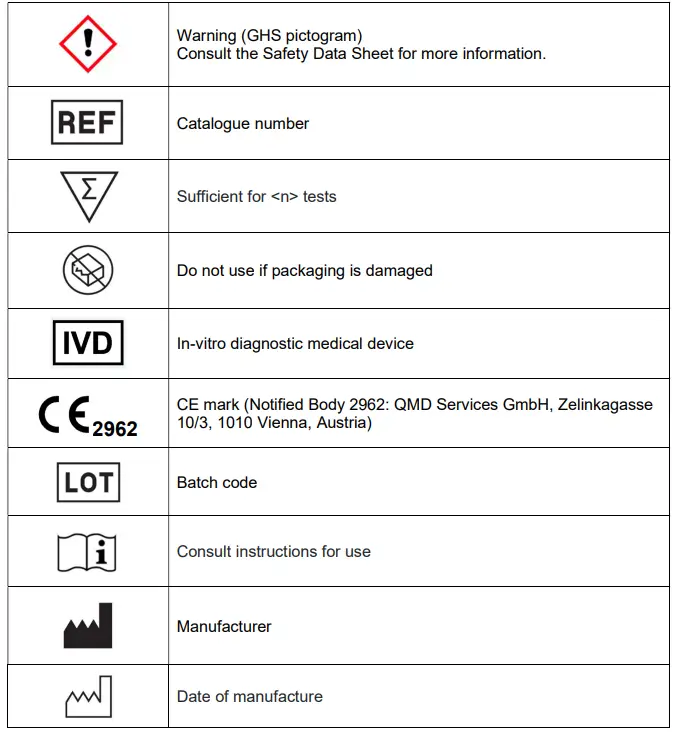
GLOSSAR DER SYMBOLE
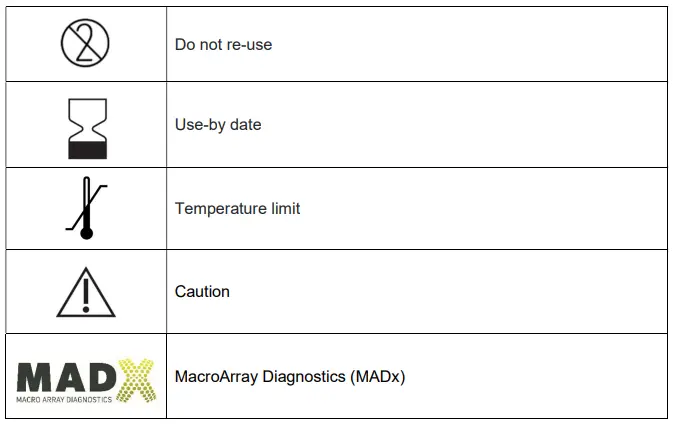
KIT-KOMPONENTEN
Jede Komponente (Reagenz) ist bis zu dem auf dem Etikett der einzelnen Komponente angegebenen Datum stabil. Es wird nicht empfohlen, Reagenzien aus verschiedenen Kitchargen zu bündeln. Eine Liste der auf dem ALEX²-Array immobilisierten Allergenextrakte und molekularen Allergene erhalten Sie von support@madx.com.
| Kit-Komponenten REF 02-2001-01 | Inhalt | Eigenschaften |
| ALEX²-Kartusche | 2 Blister à 10 ALEX² für insgesamt 20 Analysen. Kalibrierung über Masterkurve verfügbar über RAPTOR SERVER Analysesoftware. | Gebrauchsfertig. Bis zum Verfallsdatum bei 2–8 °C lagern. |
| ALEX² Sampdas Verdünnungsmittel | 1 Flasche à 9 ml | Gebrauchsfertig. Bis zum Verfallsdatum bei 2–8 °C lagern. Reagenz vor Gebrauch auf Raumtemperatur abkühlen lassen. Geöffnetes Reagenz ist bei 6–2 °C 8 Monate haltbar, enthält CCD-Inhibitor. |
| Waschlösung | 2 Flasche à 50 ml | Bereit zum Benutzen. Bis zum Verfallsdatum bei 2-8°C lagern. Lassen Sie das Reagenz vor Gebrauch Raumtemperatur erreichen. Geöffnetes Reagenz ist bei 6-2°C 8 Monate haltbar. |
| Kit-Komponenten REF 02-2001-01 | Inhalt | Eigenschaften |
| ALEX²-Nachweisantikörper | 1 Flasche à 11 ml | Bereit zum Benutzen. Bis zum Verfallsdatum bei 2-8°C lagern. Lassen Sie das Reagenz vor Gebrauch Raumtemperatur erreichen. Geöffnetes Reagenz ist bei 6-2°C 8 Monate haltbar. |
| ALEX² Substratlösung | 1 Flasche à 11 ml | Bereit zum Benutzen. Bis zum Verfallsdatum bei 2-8°C lagern. Lassen Sie das Reagenz vor Gebrauch Raumtemperatur erreichen. Geöffnetes Reagenz ist bei 6-2°C 8 Monate haltbar. |
| (ALEX²) Stop-Lösung | 1 Flasche à 2.4 ml | Gebrauchsfertig. Bis zum Verfallsdatum bei 2–8 °C lagern. Reagenz vor Gebrauch auf Raumtemperatur abkühlen lassen. Geöffnetes Reagenz ist bei 6–2 °C 8 Monate haltbar. Nach längerer Lagerung kann es zu einer trüben Lösung kommen. Dies hat keinen Einfluss auf die Ergebnisse. |
| Kit-Komponenten REF 02-5001-01 | Inhalt | Eigenschaften |
| ALEX²-Kartusche | 5 Blister à 10 ALEX² für insgesamt 50 Analysen. Kalibrierung über Masterkurve verfügbar über die RAPTOR SERVER-Analysesoftware. | Gebrauchsfertig. Bis zum Verfallsdatum bei 2–8 °C lagern. |
| ALEX² Sampdas Verdünnungsmittel | 1 Flasche à 30 ml | Gebrauchsfertig. Bis zum Verfallsdatum bei 2–8 °C lagern. Reagenz vor Gebrauch auf Raumtemperatur abkühlen lassen. Geöffnetes Reagenz ist bei 6–2 °C 8 Monate haltbar, enthält CCD-Inhibitor. |
| Waschlösung | 4 x Konz. 1 Flasche à 250 ml | Bis zum Verfallsdatum bei 2–8 °C lagern. Vor Gebrauch 1:4 mit demineralisiertem Wasser verdünnen. Reagenz vor Gebrauch auf Raumtemperatur abkühlen lassen. Geöffnetes Reagenz ist bei 6–2 °C 8 Monate haltbar. |
| ALEX²-Nachweisantikörper | 1 Flasche à 30 ml | Bereit zum Benutzen. Bis zum Verfallsdatum bei 2-8°C lagern. Lassen Sie das Reagenz vor Gebrauch Raumtemperatur erreichen. Geöffnetes Reagenz ist bei 6-2°C 8 Monate haltbar. |
| Kit-Komponenten REF 02-5001-01 | Inhalt | Eigenschaften |
| ALEX² Substratlösung | 1 Flasche à 30 ml | Gebrauchsfertig. Bis zum Verfallsdatum bei 2-8°C lagern. Reagenz vor Gebrauch auf Raumtemperatur abkühlen lassen. Geöffnetes Reagenz ist Bei 6-2°C 8 Monate haltbar. |
| (ALEX²) Stop-Lösung | 1 Flasche à 10 ml | Gebrauchsfertig. Bis zum Verfallsdatum bei 2–8 °C lagern. Reagenz vor Gebrauch auf Raumtemperatur abkühlen lassen. Geöffnetes Reagenz ist bei 6–2 °C 8 Monate haltbar. Nach längerer Lagerung kann es zu einer trüben Lösung kommen. Dies hat keinen Einfluss auf die Ergebnisse. |
ERFORDERLICHE AUSRÜSTUNG ZUR VERARBEITUNG UND ANALYSE
Manuelle Analyse
- Bildexplorer
- Arrayhalter (optional)
- Lab Rocker (Neigungswinkel 8°, benötigte Drehzahl 8 U/min)
- Inkubationskammer (BxTxH – 35x25x2 cm)
- RAPTOR SERVER Analysesoftware
- PC/Laptop
Erforderliche Ausrüstung, die nicht von MADx bereitgestellt wird:
- Demineralisiertes Wasser
- Pipetten & Spitzen (100 µl & 100 – 1000 µl)
Automatische Analyse:
- MAX-Gerät (MAX 45k oder MAX 9k)
- Waschlösung (REF 00-5003-01)
- Stopplösung (REF 00-5007-01)
- RAPTOR SERVER Analysesoftware
- PC/Laptop
Wartungsleistungen nach Herstellerangaben.
Handhabung von Arrays
Berühren Sie die Array-Oberfläche nicht. Oberflächendefekte durch stumpfe oder scharfe Gegenstände können die korrekte Ausgabe der Ergebnisse beeinträchtigen. Nehmen Sie keine ALEX²-Bilder auf, bevor das Array vollständig trocken ist (bei Raumtemperatur trocknen).
WARNHINWEISE UND VORSICHTSMASSNAHMEN
- Es wird empfohlen, bei der Vorbereitung und Handhabung von Reagenzien und s einen Hand- und Augenschutz sowie Laborkittel zu tragen und die gute Laborpraxis zu befolgenamples.
- Gemäß guter Laborpraxis sollte sämtliches menschliches Ausgangsmaterial als potenziell infektiös betrachtet und mit den gleichen Vorsichtsmaßnahmen behandelt werden wie Patientenmaterial.amples.
- ALEX² SampDas Verdünnungsmittel und die Waschlösung enthalten Natriumazid (<0.1 %) als Konservierungsmittel und müssen mit Vorsicht gehandhabt werden. Sicherheitsdatenblatt auf Anfrage erhältlich.
- Die (ALEX²) Stopplösung enthält Ethylendiamintetraessigsäure (EDTA)-Lösung und muss mit Vorsicht gehandhabt werden. Sicherheitsdatenblatt ist auf Anfrage erhältlich.
- Nur zur In-vitro-Diagnostik. Nicht zur internen oder externen Anwendung bei Menschen oder Tieren.
- Dieses Kit darf nur von in der Laborpraxis geschultem Personal verwendet werden.
- Überprüfen Sie die Kitkomponenten bei der Ankunft auf Beschädigungen. Wenn eine der Komponenten beschädigt ist (z. B. Pufferflaschen), wenden Sie sich an MADx (support@madx.com) oder Ihren Händler vor Ort. Verwenden Sie keine beschädigten Kitkomponenten, da deren Verwendung zu einer schlechten Kitleistung führen kann.
- Reagenzien nicht über ihr Verfallsdatum hinaus verwenden.
- Mischen Sie keine Reagenzien aus verschiedenen Chargen.
ELISA-VERFAHREN
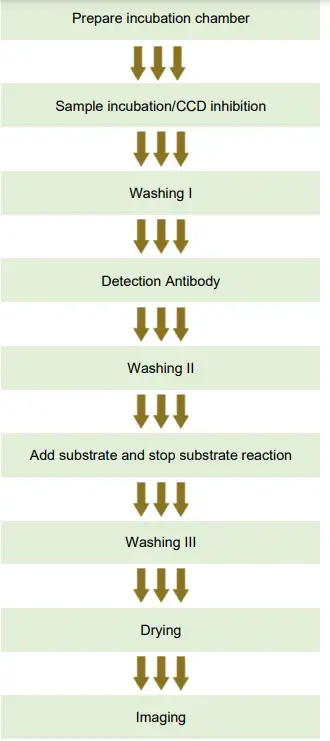
Vorbereitung
Vorbereitung von samples: Serum oder Plasma (Heparin, Citrat, kein EDTA) sampEs können Dateien aus kapillarem oder venösem Blut verwendet werden. Blut sampDateien können mit Standardverfahren gesammelt werden. Shopsamples bei 2–8°C für bis zu einer Woche. Serum und Plasma samples bei -20°C für längere Lagerung. Versand von Serum/Plasma samples bei Raumtemperatur anwendbar ist. s immer zulassenampVor Gebrauch Raumtemperatur erreichen.
Vorbereitung der Waschlösung (nur für REF 02-5001-01 und REF 00-5003-01 bei Verwendung mit MAX-Gerät): Gießen Sie den Inhalt einer Ampulle Waschlösung in den Waschbehälter des Geräts. Füllen Sie bis zur roten Markierung demineralisiertes Wasser ein und mischen Sie den Behälter mehrmals vorsichtig, ohne dass Schaum entsteht. Das geöffnete Reagenz ist bei 1-6°C 2 Monate haltbar.
Inkubationskammer: Schließen Sie den Deckel während aller Testschritte, um einen Abfall der Luftfeuchtigkeit zu verhindern.
Parameter of Verfahren:
- 100 µl sample + 400 µl ALEX² Sampdas Verdünnungsmittel
- 500 µl ALEX² Nachweisantikörper
- 500 µl ALEX² Substratlösung
- 100 µl (ALEX²) Stopplösung
- 4500 µl Waschlösung
Die Testdauer beträgt etwa 3 Stunden und 30 Minuten (ohne Trocknen des verarbeiteten Arrays).
Es wird nicht empfohlen, mehr Tests durchzuführen, als in 8 Minuten pipettiert werden können. Alle Inkubationen werden bei Raumtemperatur (20–26 °C) durchgeführt.
Alle Reagenzien sind bei Raumtemperatur (20-26°C) zu verwenden. Der Test darf nicht in direktem Sonnenlicht durchgeführt werden.
Inkubationskammer vorbereiten
Öffnen Sie die Inkubationskammer und legen Sie Papiertücher auf den Boden. Tränken Sie die Papiertücher mit demineralisiertem Wasser, bis keine trockenen Stellen mehr auf den Papiertüchern sichtbar sind.
Sample Inkubation/CCD-Hemmung
Entnehmen Sie die benötigte Anzahl ALEX²-Kartuschen und legen Sie diese in den Array-Halter. Fügen Sie 400 μl ALEX² S hinzu.ample Diluent zu jeder Patrone. Fügen Sie 100 μl Patientensample zu den Kartuschen. Stellen Sie sicher, dass die resultierende Lösung gleichmäßig verteilt ist. Legen Sie die Kartuschen in die vorbereitete Inkubationskammer und stellen Sie die Inkubationskammer mit den Kartuschen auf die Laborwippe, sodass die Kartuschen entlang der langen Seite der Kartusche wippen. Starten Sie die Seruminkubation mit 8 U/min für 2 Stunden. Schließen Sie die Inkubationskammer, bevor Sie die Laborwippe starten. Entladen Sie nach 2 Stunden das SerumampDateien in einen Sammelbehälter. Wischen Sie Tropfen vorsichtig mit einem Papiertuch von der Patrone ab.
Vermeiden Sie das Berühren der Array-Oberfläche mit dem Papiertuch! Vermeiden Sie jegliche Verschleppung oder Kreuzkontamination vonampDateien zwischen einzelnen ALEX²-Kassetten!
Optionaler oder positiver Hom s LF (CCD-Marker): mit dem Standard-CCD-Antikörperhemmungsprotokoll (wie in Abschnitt 2 beschrieben: sample Inkubation/CCD-Hemmung) beträgt die CCD-Hemmungseffizienz 85 %. Wenn eine höhere Hemmungseffizienz erforderlich ist, bereiten Sie eine 1 ml sample-Röhrchen, 400 μl ALEX² S zugebenample Verdünnungsmittel und 100 μl Serum. 30 Minuten lang inkubieren (ohne Schütteln) und dann mit dem üblichen Testverfahren fortfahren.
Notiz: Der zusätzliche CCD-Hemmungsschritt führt in vielen Fällen zu einer Hemmrate für CCD-Antikörper von über 95 %.
1a. Waschen I
Geben Sie 500 μl Waschlösung in jede Kartusche und inkubieren Sie diese 8 Minuten lang auf dem Laborwippentisch (bei 5 U/min). Lassen Sie die Waschlösung in einen Auffangbehälter ab und klopfen Sie die Kartuschen kräftig auf einem Stapel trockener Papiertücher aus. Wischen Sie verbleibende Tropfen vorsichtig mit einem Papiertuch von den Kartuschen ab.
Wiederholen Sie diesen Schritt noch 2 Mal.
Nachweisantikörper hinzufügen
Geben Sie jeder Kartusche 500 µl ALEX² Detection Antibody hinzu.
Stellen Sie sicher, dass die gesamte Array-Oberfläche mit der ALEX² Detection Antibody-Lösung bedeckt ist.
Legen Sie die Kartuschen in die Inkubationskammer auf dem Laborwippentisch und inkubieren Sie sie 8 Minuten lang bei 30 U/min. Lassen Sie die Nachweisantikörperlösung in einen Auffangbehälter ab und klopfen Sie die Kartuschen kräftig auf einem Stapel trockener Papiertücher aus. Wischen Sie verbleibende Tropfen vorsichtig mit einem Papiertuch von den Kartuschen ab.
2a. Waschen II
Geben Sie 500 μl Waschlösung in jede Kartusche und inkubieren Sie diese 8 Minuten lang bei 5 U/min auf der Laborwippe. Lassen Sie die Waschlösung in einen Auffangbehälter ab und klopfen Sie die Kartuschen kräftig auf einem Stapel trockener Papiertücher aus. Wischen Sie verbleibende Tropfen vorsichtig mit einem Papiertuch von den Kartuschen ab.
Wiederholen Sie diesen Schritt noch 4 Mal.
3+4. ALEX² Substratlösung hinzufügen und Substratreaktion stoppen
Geben Sie 500 μl ALEX²-Substratlösung in jede Kartusche. Starten Sie einen Timer mit dem Befüllen der ersten Kartusche und fahren Sie mit dem Befüllen der restlichen Kartuschen fort. Stellen Sie sicher, dass die gesamte Array-Oberfläche mit der Substratlösung bedeckt ist, und inkubieren Sie die Arrays genau 8 Minuten lang ohne zu schütteln (Laborwippe bei 0 U/min und in horizontaler Position).
Nach genau 8 Minuten geben Sie 100 μl der (ALEX²)-Stopplösung in alle Kartuschen, beginnend mit der ersten Kartusche, um sicherzustellen, dass alle Arrays gleich lange mit der ALEX²-Substratlösung inkubiert werden. Schütteln Sie die (ALEX²)-Stopplösung vorsichtig, um sie gleichmäßig in den Array-Kartuschen zu verteilen, nachdem die (ALEX²)-Stopplösung auf alle Arrays pipettiert wurde. Entleeren Sie anschließend die (ALEX²)-Substrat-/Stopplösung aus den Kartuschen und klopfen Sie die Kartuschen kräftig auf einem Stapel trockener Papiertücher aus. Wischen Sie alle verbleibenden Tropfen vorsichtig mit einem Papiertuch von den Kartuschen ab.
Der Lab Rocker darf während der Substratinkubation NICHT SCHÜTTELN!
4a. Waschen III
Geben Sie 500 μl Waschlösung in jede Kartusche und inkubieren Sie sie 8 Sekunden lang bei 30 U/min auf der Laborwippe. Lassen Sie die Waschlösung in einen Auffangbehälter ab und klopfen Sie die Kartuschen kräftig auf einem Stapel trockener Papiertücher aus. Wischen Sie alle verbleibenden Tropfen vorsichtig mit einem Papiertuch von den Kartuschen ab.
Bildanalyse
Lassen Sie die Arrays nach Abschluss des Testverfahrens bei Raumtemperatur an der Luft trocknen, bis sie vollständig trocken sind (kann bis zu 45 Minuten dauern).
Die vollständige Trocknung ist für die Empfindlichkeit des Tests von entscheidender Bedeutung. Nur vollständig getrocknete Arrays bieten ein optimales Signal-Rausch-Verhältnis.
Abschließend werden die getrockneten Arrays mit dem ImageXplorer oder einem MAX-Gerät gescannt und mit der RAPTOR SERVER-Analysesoftware analysiert (Details finden Sie im Handbuch zur RAPTOR SERVER-Software). Die RAPTOR SERVER-Analysesoftware wird nur in Kombination mit dem ImageXplorer-Instrument und den MAX-Geräten verifiziert. Daher übernimmt MADx keine Verantwortung für Ergebnisse, die mit anderen Bilderfassungsgeräten (wie Scannern) erzielt wurden.
Assay-Kalibrierung
Die ALEX²-Masterkalibrierungskurve wurde durch Referenztests mit Serumpräparaten mit spezifischem IgE gegen verschiedene Antigene erstellt, die den beabsichtigten Messbereich abdecken. Chargenspezifische Kalibrierungsparameter werden von der RAPTOR SERVER-Analysesoftware bereitgestellt. ALEX²-sIgE-Testergebnisse werden als kUA/l ausgedrückt. Gesamt-IgE-Ergebnisse sind halbquantitativ und werden aus einer Anti-IgE-Messung mit chargenspezifischen Kalibrierungsfaktoren berechnet, die von der RAPTOR SERVER-Analysesoftware bereitgestellt und entsprechend den chargenspezifischen QR-Codes ausgewählt werden.
Die Kurvenparameter für jede Charge werden durch ein internes Referenztestsystem anhand von Serumpräparaten angepasst, die auf ImmunoCAP (Thermo Fisher Scientific) auf spezifisches IgE gegen verschiedene Allergene getestet wurden. Die ALEX²-Ergebnisse sind daher indirekt auf das WHO-Referenzpräparat 11/234 für Gesamt-IgE rückführbar.
Systematische Schwankungen der Signalstärke zwischen den Chargen werden durch heterologe Kalibrierung anhand einer IgE-Referenzkurve normalisiert. Ein Korrekturfaktor wird verwendet, um chargenspezifische Messabweichungen systematisch auszugleichen.
Messbereich
Spezifisches IgE: 0.3-50 kUA/l quantitativ
Gesamt-IgE: 20-2500 kU/l semiquantitativ
QUALITÄTSKONTROLLE
Aufzeichnungen für jeden Assay
Gemäß der guten Laborpraxis wird empfohlen, die Chargennummern aller verwendeten Reagenzien aufzuzeichnen.
Kontrollproben
Nach guter Laborpraxis wird empfohlen, Qualitätskontrollen sampDie Proben werden in definierten Intervallen aufgenommen. Referenzwerte für bestimmte im Handel erhältliche Kontrollseren können auf Anfrage von MADx bereitgestellt werden.
DATENANALYSE
Zur Bildanalyse der verarbeiteten Arrays wird der ImageXplorer oder ein MAX-Gerät verwendet. ALEX²-Bilder werden automatisch mit der RAPTOR SERVER-Analysesoftware analysiert und ein Bericht erstellt, der die Ergebnisse für den Benutzer zusammenfasst.
ERGEBNISSE
ALEX² ist ein quantitativer ELISA-Test für spezifisches IgE und eine semiquantitative Methode für Gesamt-IgE. Allergenspezifische IgE-Antikörper werden als IgE-Reaktionseinheiten (kUA/l) ausgedrückt, Gesamt-IgE-Ergebnisse als kU/l. Die RAPTOR SERVER-Analysesoftware berechnet und meldet automatisch sIgE-Ergebnisse (quantitativ) und tIgE-Ergebnisse (semiquantitativ).
EINSCHRÄNKUNGEN DES VERFAHRENS
Eine definitive klinische Diagnose sollte von medizinischem Fachpersonal nur in Verbindung mit allen verfügbaren klinischen Befunden gestellt werden und nicht nur auf den Ergebnissen einer einzigen Diagnosemethode basieren.
In bestimmten Anwendungsbereichen (z. B. Nahrungsmittelallergien) können zirkulierende IgE-Antikörper möglicherweise nicht nachweisbar sein, obwohl eine klinische Manifestation einer Nahrungsmittelallergie gegen ein bestimmtes Allergen vorliegt. Dies liegt daran, dass diese Antikörper spezifisch für Allergene sein können, die während der industriellen Verarbeitung, beim Kochen oder bei der Verdauung verändert werden und daher in dem ursprünglichen Nahrungsmittel, auf das der Patient getestet wird, nicht vorhanden sind.
Negative Ergebnisse beim Insektengifttest weisen lediglich auf nicht nachweisbare Werte giftspezifischer IgE-Antikörper hin (z. B. aufgrund längerer Nichtexposition) und schließen das Vorhandensein einer klinischen Überempfindlichkeit gegenüber Insektenstichen nicht aus.
Bei Kindern, insbesondere im Alter bis 2 Jahre, ist der Normbereich des tIgE niedriger als bei Jugendlichen und Erwachsenen [7]. Daher ist zu erwarten, dass bei einem höheren Anteil von Kindern unter 2 Jahren der Gesamt-IgE-Spiegel unterhalb der angegebenen Nachweisgrenze liegt. Für die spezifische IgE-Messung gilt diese Einschränkung nicht.
ERWARTETE WERTE
Der enge Zusammenhang zwischen allergenspezifischen IgE-Antikörperspiegeln und allergischen Erkrankungen ist gut bekannt und in der Literatur ausführlich beschrieben [1]. Jeder sensibilisierte Patient weist einen individuellen IgE-Profile bei einem Test mit ALEX². Die IgE-Antwort mit sampDie Werte gesunder, nicht allergischer Personen liegen bei einzelnen molekularen Allergenen und Allergenextrakten unter 0.3 kU/l, wenn sie mit ALEX² getestet werden. Der Referenzbereich für Gesamt-IgE bei Erwachsenen liegt bei < 100 kU/l. Die gute Laborpraxis empfiehlt, dass jedes Labor seinen eigenen Bereich erwarteter Werte festlegt.
LEISTUNGSMERKMALE
Die Leistungsmerkmale sowie die Zusammenfassung der Sicherheits- und Leistungsdaten finden Sie auf der MADx webWebsite: https://www.madx.com/extras.
GARANTIE
Die Leistungsdaten wurden mit dem in dieser Gebrauchsanweisung beschriebenen Verfahren ermittelt. Jede Änderung oder Modifikation des Verfahrens kann die Ergebnisse beeinflussen, und MacroArray Diagnostics lehnt in einem solchen Fall alle ausdrücklichen Gewährleistungen (einschließlich der stillschweigenden Gewährleistung der Marktgängigkeit und Eignung für den Gebrauch) ab. Folglich haften MacroArray Diagnostics und seine lokalen Vertriebshändler in einem solchen Fall nicht für indirekte oder Folgeschäden.
ABKÜRZUNGEN
| ALEX | Allergie-Experte |
| CCD | Kreuzreaktive Kohlenhydratdeterminanten |
| EDTA | Ethylendiamintetraessigsäure |
| ELISA | Enzymgekoppelter Immunadsorptionstest |
| IgE | Immunglobulin E |
| IVD | In-vitro-Diagnostik |
| kU/l | Kilo-Einheiten pro Liter |
| kUA/l | Kiloeinheiten allergenspezifisches IgE pro Liter |
| MADx | MacroArray-Diagnose |
| Referenz | Referenznummer |
| U/min | Runden pro Minute |
| sIgE | Allergenspezifisches IgE |
| tIgE | Gesamt-IgE |
| ul | Mikroliter |
ALLERGENLISTE ALEX²
Allergenextrakte: Aca m, Aca s, Ach d, Ail a, All c, All s, Ama r, Amb a, Ana o, Api m, Art v, Ave s, Ber e, Bos d Fleisch, Bos d Milch, Bro p, Cam d, Can f ♂ Urin, Can s, Cap a, Cap h Epithelien, Cap h Milch, Car c, Car i, Car p, Che a, Che q, Chi spp., Cic a, Cit s, Cla h, Clu h, Cor a Pollen, Cuc p, Cup s, Cyn d, Dau c, Dol spp., Equ c Milch, Equ c Fleisch, Fag e, Fic b, Fic c, Fra e, Gad m, Gal d Fleisch, Gal d Weiß, Gal d Eigelb, Hel a, Hom g, Hor v, Jug r, Jun a, Len c, Lit s, Loc m, Lol spp., Lup a, Mac i, Man i, Mel g, Mor r, Mus a, Myt e, Ori v, Ory Fleisch, Ory s, Ost e, Ovi a Epithelien, Ovi a Fleisch, Ovi a Milch, Pan b, Pan m, Pap s, Par j, Pas n, Pec spp., Pen ch, Per a, Pers a, Pet c, Pha v, Phr c, Pim a, Pis s, Pla l, Pol d, Pop n, Pru av, Pru du, Pyr c, Raj c, Rat n, Rud spp., Sac c, Sal k, Sal s, Sco s, Sec c Mehl, Sec c Pollen, Ses i, Sin, Sol spp., Sola l, Sol t, Sus d Epithel, Sus d Fleisch, Ten m, Thu a, Tri fo, Tri s, Tyr p, Ulm c, Urt d, Vac m, Ves v, Zea m Mehl
Gereinigte natürliche Bestandteile: nAct d 1, nApi m 1, nAra h 1, nAra h 3, nBos d 4, nBos d 5, nBos d 6, nBos d 8, nCan f 3, nCor a 9, nCor a 11, nCup a 1, nCry j 1, nEqu c 3, nFage 2, nGad m 1, nGad m 2 + 3, nGal d 2, nGal d 3, nGal d 4, nGal d 5, nGly m 5, nGly m 6, nJug r 4, nMac i 2S-Albumin, nOle e 7 (RUO), nPap s 2S-Albumin, nPis v 3, nPla eine 2, nTri eine aA_TI
Rekombinante Komponenten: rAct d 10, rAct d 2, rAct d 5, rAln g 1, rAln g 4, rAlt a 1, rAlt a 6, rAmb a 1, rAmb a 4, rAna o 2, rAna o 3, rAni s 1, rAni s 3, rApi g 1, rApi g 2, rApi g 6, rApi m 10, rAra h 2, rAra h 6, rAra h 8, rAra h 9, rAra h 15, rArg r 1, rArt v 1, rArt v 3, Raspel f 1, Raspel f 3, Raspel f 4, Raspel f 6, rBer e 1, rBet v 1, rBet v 2, rBet v 6, rBla g 1, rBla g 2, rBla g 4, rBla g 5, rBla g 9, rBlo t 10, rBlo t 21, rBlo t 5, rBos d 2, rCan f 1, rCan f 2, rCan f 4, rCan f 6, rCan f Fel d 1 wie, rCan s 3, rCav p 1, rChe a 1, rCla h 8, rClu h 1, rCor a 1.0103, rCor a 1.0401 , rCor a 8, rCor a 12 (RUO), rCor a 14, rCra c 6, , rCuc m 2, rCyn d 1, rCyp c 1, rDau c 1, rDer f 1, rDer f 2, rDer p 1, rDer p 10, rDer p 11, rDer p 2, rDer p 20, rDer p 21, rDer p 23, rDer p 5, rDer p 7, rEqu c 1, rEqu c 4, rFag s 1, rFel d 1, rFel d 2, rFel d 4, rFel d 7, rFra a 1 + 3, rFra e 1, rGal d 1, rGly d 2, rGly m 4, rGly m 8, rHev b 1, rHev b 3, rHev b 5, rHev b 6.02, rHev b 8, rHev b 11, rHom s LF, rJug r 1, rJug r 2, rJug r 3, rJug r 6, rLep d 2, rLol p 1, rMal d 1, rMal d 3, rMala s 11, rMala s 5, rMala s 6, rMal d 2, rMer a 1, rMes a 1 (RUO), rMus m 1, rOle e 1, rOle 9, rOry c 1, rOry c 2, rOry c 3, rPar j 2, rPen m 1, rPen m 2, rPen m 3, rPen m 4, rPer a 7, rPhl p 1, rPhl p 12, rPhl p 2, rPhl p 5.0101, rPhl p 6, rPhl p 7, rPho d 2, rPhod s 1, rPis v 1, rPis v 2 , rPis v 4 (RUO), rPla a 1, rPla a 3, rPla l 1, rPol d 5, rPru p 3, rPru p 7 (RUO), rRaj c Parvalbumin, rSal k 1, rSal s 1, rSco s 1 , rses i 1, rSin a 1, rSola l 6, rSus d 1, rThu a 1, rTri a 14, rTri a 19, rTyr p 2, rVes v 1, rVes v 5, rVit v 1, rXip g 1, rZea m 14
REFERENZEN
- Hamilton, RG. (2008). Beurteilung menschlicher allergischer Erkrankungen. Klinische Immunologie. 1471-1484. 10.1016/B978-0-323-04404-2.10100-9.
- Harwanegg C, Laffer S, Hiller R, Mueller MW, Kraft D, Spitzauer S, Valenta R. Mikroarray-basierte rekombinante Allergene zur Allergiediagnostik. Clin Exp Allergy. 2003 Jan;33(1):7-13. doi: 10.1046/j.1365-2222.2003.01550.x. PMID: 12534543.
- Hiller R, Laffer S, Harwanegg C, Huber M, Schmidt WM, Twardosz A, Barletta B, Becker WM, Blaser K, Breiteneder H, Chapman M, Crameri R, Duchêne M, Ferreira F, Fiebig H, Hoffmann-Sommergruber K, King TP, Kleber-Janke T, Kurup VP, Lehrer SB, Lidholm J, Müller U, Pini C, Reese G, Scheiner O, Scheynius A, Shen HD, Spitzauer S, Suck R, Swoboda I, Thomas W, Tinghino R, Van Hage-Hamsten M, Virtanen T, Kraft D, Müller MW, Valenta R. Mikroarrayierte Allergenmoleküle: diagnostische Gatekeeper für die Allergiebehandlung. FASEB J. 2002 Mar;16(3):414-6. doi: 10.1096/fj.01-0711fje. Epub 2002 Januar 14. PMID: 11790727
- Ferrer M, Sanz ML, Sastre J, Bartra J, del Cuvillo A, Montoro J, Jáuregui I, Dávila I, Mullol J, Valero A. Molekulare Diagnostik in der Allergologie: Anwendung der Microarray-Technik. J Investig Allergol Clin Immunol. 2009;19 Suppl 1:19-24. PMID: 19476050.
- Ott H, Fölster-Holst R, Merk HF, Baron JM. Allergen-Microarrays: ein neues Werkzeug für hochauflösendes IgE-Profiling bei Erwachsenen mit atopischer Dermatitis. Eur J Dermatol. 2010 Jan-Feb;20(1):54-
61. doi: 10.1684/ejd.2010.0810. Epub 2009, 2. Oktober. PMID: 19801343. - Sastre J. Molekulare Diagnostik bei Allergien. Clin Exp Allergy. 2010 Okt;40(10):1442-60. doi: 10.1111/j.1365-2222.2010.03585.x. Epub 2010 Aug 2. PMID: 20682003.
- Martins TB, Bandhauer ME, Bunker AM, Roberts WL, Hill HR. Neue Referenzintervalle für Gesamt-IgE bei Kindern und Erwachsenen. J Allergy Clin Immunol. 2014 Feb;133(2):589-91.
Einzelheiten zu den durchgeführten analytischen und klinischen Studien finden Sie in den Leistungsbeschreibungen unter https://www.madx.com/extras.
GESCHICHTE VERÄNDERN
| Version | Beschreibung | Ersetzt |
| 11 | nGal d1 wurde in rGal d1 geändert; URL aktualisiert auf www.madx.com; CE ergänzt um die Nummer der Benannten Stelle; Änderungshistorie hinzugefügt | 10 |

© Copyright von MacroArray Diagnostics
MacroArray-Diagnose (MADx)
Lemböckgasse 59, Top 4
1230 Wien, Österreich
+43 (0)1 865 2573
www.madx.com
Versionsnummer: 02-IFU-01-DE-11 Veröffentlicht: 09-2024
Kurzanleitung
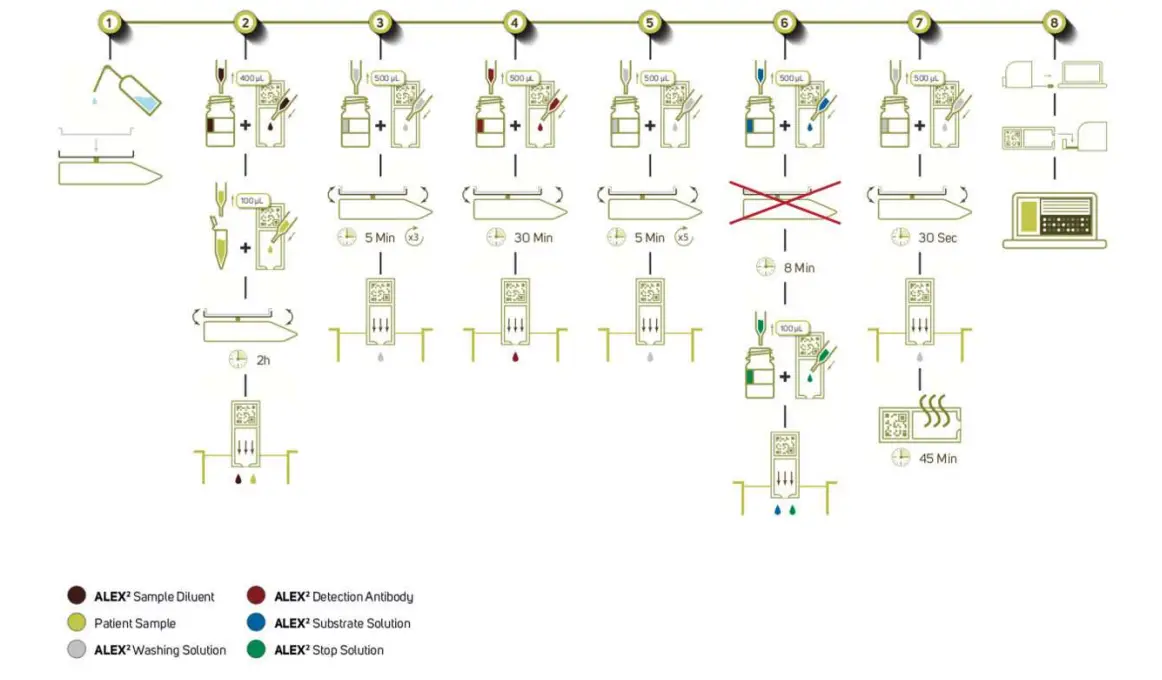
MacroArray-Diagnose
Lemböckgasse 59, Top 4
1230 Wien
www.madx.com
CRN 448974 g
Dokumente / Ressourcen
 | MacroArray ALLERGY XPLORER Makro-Array-Diagnostik [pdf] Anweisungen 91201229202JQ, 02-2001-01, 02-5001-01, ALLERGY XPLORER Makro-Array-Diagnostik, ALLERGY XPLORER, Makro-Array-Diagnostik, Array-Diagnostik, Diagnostik |




