MacroArray ALLERGY XPLORER Diagnostyka MacroArray
Specyfikacje
- Nazwa produktu: Podstawowy UDI-DI 91201229202JQ
- Numery referencyjne: REF 02-2001-01, 02-5001-01
- Przeznaczenie: Ilościowe oznaczanie swoistych dla alergenów IgE (sIgE) oraz półilościowe oznaczanie całkowitego IgE (tIgE)
- Użytkownicy: Przeszkolony personel laboratoryjny i personel medyczny w laboratorium medycznym
- Przechowywanie: Odczynniki zestawu są stabilne przez 6 miesięcy po otwarciu
Instrukcje użytkowania produktu
Zasada postępowania
Produkt pozwala na ilościowe wykrywanie swoistych dla alergenów IgE oraz półilościowe wykrywanie całkowitych IgE.
Wysyłka i magazynowanie
Należy upewnić się, że odczynniki zestawu są przechowywane zgodnie z zaleceniami i zostaną zużyte w ciągu 6 miesięcy od otwarcia.
Utylizacja odpadów:
Postępuj zgodnie z właściwymi procedurami utylizacji odpadów, zgodnie z przepisami.
Elementy zestawu
Szczegółowe informacje na temat elementów zestawu można znaleźć w instrukcji obsługi.
Wymagany sprzęt
Analiza ręczna: Upewnij się, że posiadasz niezbędny sprzęt dostarczony przez producenta.
Automatyczna analiza: Użyj urządzenia MAX, Washing Solution, Stop Solution, RAPTOR SERVER Analysis Software i PC/Laptop. Postępuj ściśle według instrukcji konserwacji.
Obsługa tablic
Aby uzyskać dokładne wyniki, należy postępować zgodnie z instrukcjami dotyczącymi obchodzenia się z tablicami.
Ostrzeżenia i środki ostrożności
- Należy nosić odpowiedni sprzęt ochronny, taki jak okulary i dłonie oraz fartuchy laboratoryjne.
- Obsługa odczynników i sampprzestrzegając dobrych praktyk laboratoryjnych.
- Wszystkie materiały pochodzenia ludzkiego należy traktować jako potencjalnie zakaźne i obchodzić się z nimi ostrożnie.
Często zadawane pytania
- P: Jak długo odczynniki zestawu zachowują stabilność?
A: Odczynniki zestawu zachowują stabilność przez 6 miesięcy po otwarciu, pod warunkiem przechowywania w określonych warunkach. - P: Kto może używać tego produktu?
A: Produkt ten jest przeznaczony do stosowania przez przeszkolony personel laboratoryjny i personel medyczny w laboratoriach medycznych.
www.madx.com
ALLERGY XPLORER (ALEX²) INSTRUKCJA STOSOWANIA
OPIS
Allergy Xplorer (ALEX²) to test diagnostyczny in vitro oparty na teście immunoenzymatycznym (ELISA) służący do ilościowego pomiaru stężenia alergenowo swoistych IgE (sIgE).
Niniejsza instrukcja użytkowania dotyczy następujących produktów:
| Podstawowe UDI-DI | ODNOŚNIK | Produkt |
| 91201229202JQ | 02-2001-01 | ALEX² dla 20 analiz |
| 02-5001-01 | ALEX² dla 50 analiz |
PRZEZNACZENIE
ALEX² Allergy Xplorer to zestaw testowy służący do badania in vitro surowicy lub osocza ludzkiego (z wyjątkiem osocza EDTA) w celu uzyskania informacji ułatwiających diagnozę pacjentów cierpiących na choroby IgE-zależne w połączeniu z innymi wynikami klinicznymi lub wynikami testów diagnostycznych.
Urządzenie medyczne IVD wykrywa alergenowo swoiste IgE (sIgE) ilościowo i całkowite IgE (tIgE) półilościowo. Produkt jest używany przez przeszkolony personel laboratoryjny i personel medyczny w laboratorium medycznym.
PODSUMOWANIE I WYJAŚNIENIE TESTU
Reakcje alergiczne to natychmiastowe reakcje nadwrażliwości typu I, które są pośredniczone przez przeciwciała należące do klasy immunoglobulin IgE. Po narażeniu na określone alergeny, pośredniczone przez IgE uwalnianie histaminy i innych mediatorów z komórek tucznych i bazofilów powoduje objawy kliniczne, takie jak astma, alergiczny nieżyt nosa i spojówek, atopowe zapalenie skóry i objawy żołądkowo-jelitowe [1]. Dlatego szczegółowy wzór uczulenia na określone alergeny pomaga w ocenie pacjentów z alergią [2-6]. Nie ma ograniczeń co do populacji testowej. Podczas opracowywania testów IgE wiek i płeć zazwyczaj nie są uważane za czynniki krytyczne, ponieważ poziomy IgE, które są mierzone w tych testach, nie różnią się znacząco w zależności od tych danych demograficznych.
ALEX² obejmuje wszystkie główne źródła alergenów typu I. Pełną listę ekstraktów alergenów ALEX² i alergenów molekularnych można znaleźć na dole tej instrukcji.
Ważna informacja dla użytkownika!
Aby prawidłowo używać ALEX², konieczne jest, aby użytkownik uważnie przeczytał i przestrzegał niniejszej instrukcji użytkowania. Producent nie ponosi żadnej odpowiedzialności za jakiekolwiek użycie tego systemu testowego, które nie zostało opisane w tym dokumencie, ani za modyfikacje systemu testowego dokonane przez użytkownika.
Uwaga: Wariant zestawu 02-2001-01 testu ALEX² (20 tablic) jest przeznaczony wyłącznie do ręcznego przetwarzania. Aby użyć tego wariantu zestawu ALEX² z automatycznym MAX 9k, należy zamówić osobno roztwór myjący (REF 00-5003-01) i roztwór zatrzymujący (REF 00-5007-01). Wszystkie dalsze informacje o produkcie można znaleźć w odpowiedniej instrukcji użytkowania: https://www.madx.com/extras.
Zestaw ALEX² w wersji 02-5001-01 (50 tablic) można stosować do automatycznego przetwarzania z urządzeniem MAX 9k (REF 17-0000-01) oraz MAX 45k (REF 16-0000-01).
ZASADA PROCEDURY
ALEX² to test immunoenzymatyczny oparty na teście immunoenzymatycznym (ELISA). Ekstrakty alergenów lub alergeny molekularne, które są sprzężone z nanocząsteczkami, są osadzane w sposób systematyczny na fazie stałej, tworząc makroskopową matrycę. Najpierw alergeny związane z cząsteczkami reagują ze swoistym IgE obecnym w osoczu pacjenta.ample. Po inkubacji nieswoiste IgE jest wypłukiwane. Procedura jest kontynuowana przez dodanie znakowanego enzymem przeciwciała wykrywającego IgE antyludzkie, które tworzy kompleks z cząsteczkowo związanym swoistym IgE. Po drugim etapie płukania dodawany jest substrat, który jest przekształcany w nierozpuszczalny, kolorowy osad przez związany z przeciwciałem enzym. Na koniec reakcja enzym-substrat jest zatrzymywana przez dodanie odczynnika blokującego. Ilość osadu jest proporcjonalna do stężenia swoistego IgE w s pacjentaample. Po procedurze testu laboratoryjnego następuje akwizycja obrazu i analiza przy użyciu systemu ręcznego (ImageXplorer) lub automatycznego (MAX 45k lub MAX 9k). Wyniki testu są analizowane za pomocą oprogramowania RAPTOR SERVER Analysis Software i podawane w jednostkach odpowiedzi IgE (kUA/l). Całkowite wyniki IgE są również podawane w jednostkach odpowiedzi IgE (kU/l). RAPTOR SERVER jest dostępny w wersji 1, aby uzyskać pełny czterocyfrowy numer wersji, zapoznaj się z nadrukiem RAPTOR SERVER dostępnym pod adresem www.raptor-server.com/odcisk.
WYSYŁKA I PRZECHOWYWANIE
Wysyłka ALEX² odbywa się w warunkach temperatury otoczenia. Niemniej jednak zestaw musi być przechowywany natychmiast po dostarczeniu w temperaturze 2-8°C. Prawidłowo przechowywany ALEX² i jego komponenty mogą być używane do wskazanej daty ważności.
Odczynniki zestawu zachowują trwałość przez 6 miesięcy po otwarciu (we wskazanych warunkach przechowywania).
UTYLIZACJA ODPADÓW
Zużyty wkład ALEX² i nieużywane elementy zestawu należy wyrzucić razem z odpadami chemicznymi z laboratorium. Należy przestrzegać wszystkich krajowych, stanowych i lokalnych przepisów dotyczących utylizacji.
SŁOWNIK SYMBOLI
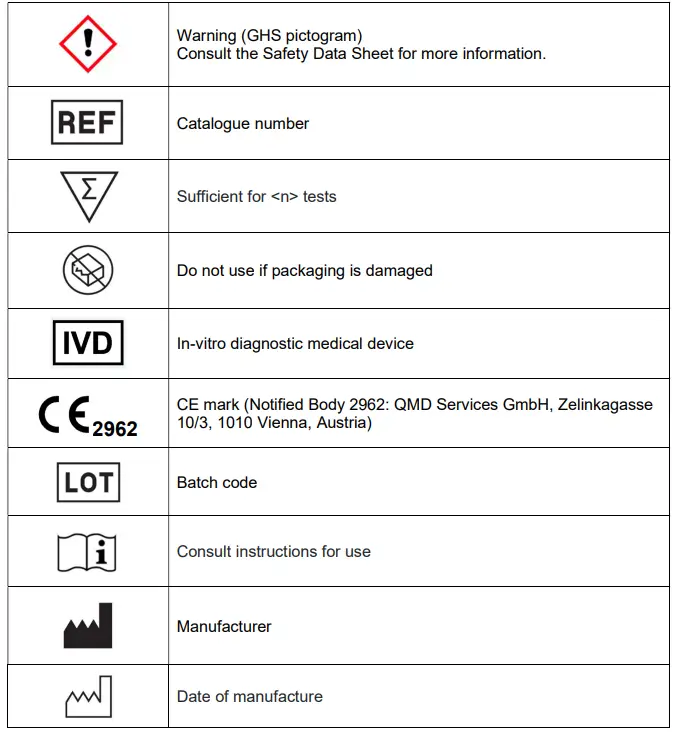
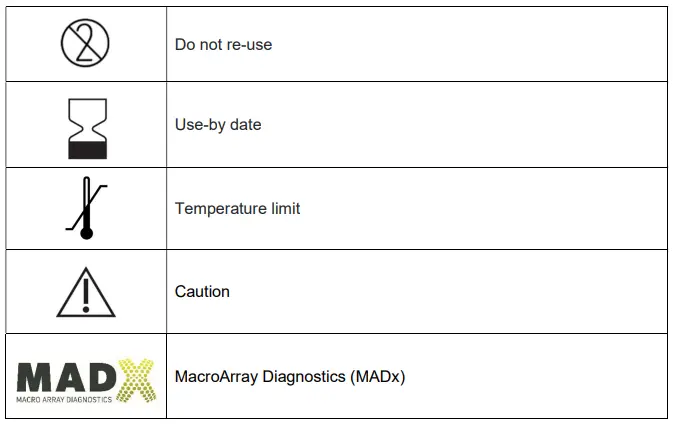
SKŁADNIKI ZESTAWU
Każdy składnik (odczynnik) jest stabilny do daty podanej na etykiecie każdego pojedynczego składnika. Nie zaleca się łączenia żadnych odczynników z różnych partii zestawu. Aby uzyskać listę ekstraktów alergenów i alergenów molekularnych unieruchomionych na macierzy ALEX², skontaktuj się z wsparcie@madx.com.
| Elementy zestawu REF 02-2001-01 | Treść | Właściwości |
| Wkład ALEX² | 2 blistry po 10 ALEX² na łącznie 20 analiz.
Kalibracja za pomocą krzywej głównej dostępna poprzez RAPTOR SERVER Oprogramowanie analityczne. |
Gotowe do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. |
| ALEX² SampRozcieńczalnik | 1 butelka po 9 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik należy pozostawić do osiągnięcia temperatury pokojowej. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C, zawiera inhibitor CCD. |
| Roztwór do prania | 2 butelka po 50 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik powinien osiągnąć temperaturę pokojową. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. |
| Elementy zestawu REF 02-2001-01 | Treść | Właściwości |
| Przeciwciało wykrywające ALEX² | 1 butelka po 11 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik powinien osiągnąć temperaturę pokojową. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. |
| Rozwiązanie podłoża ALEX² | 1 butelka po 11 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik powinien osiągnąć temperaturę pokojową. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. |
| (ALEX²) Rozwiązanie zatrzymujące | 1 butelka po 2.4 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik należy pozostawić do osiągnięcia temperatury pokojowej. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. Po dłuższym przechowywaniu może wyglądać jak mętny roztwór. Nie ma to wpływu na wyniki. |
| Elementy zestawu REF 02-5001-01 | Treść | Właściwości |
| Wkład ALEX² | 5 blistry po 10 ALEX² na łącznie 50 analiz.
Kalibracja za pomocą krzywej wzorcowej dostępna za pośrednictwem oprogramowania analitycznego RAPTOR SERVER. |
Gotowe do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. |
| ALEX² SampRozcieńczalnik | 1 butelka po 30 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik należy pozostawić do osiągnięcia temperatury pokojowej. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C, zawiera inhibitor CCD. |
| Roztwór do prania | 4 x stęż. 1 butelka po 250 ml | Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem rozcieńczyć 1 do 4 wodą demineralizowaną. Przed użyciem odczynnik należy pozostawić do osiągnięcia temperatury pokojowej. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. |
| Przeciwciało wykrywające ALEX² | 1 butelka po 30 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik powinien osiągnąć temperaturę pokojową. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. |
| Elementy zestawu REF 02-5001-01 | Treść | Właściwości |
| Rozwiązanie podłoża ALEX² | 1 butelka po 30 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik należy pozostawić do osiągnięcia temperatury pokojowej. Otwarty odczynnik jest
zachowuje stabilność przez 6 miesięcy w temperaturze 2-8°C. |
| (ALEX²) Rozwiązanie zatrzymujące | 1 butelka po 10 ml | Gotowy do użycia. Przechowywać w temperaturze 2-8°C do daty ważności. Przed użyciem odczynnik należy pozostawić do osiągnięcia temperatury pokojowej. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C. Po dłuższym przechowywaniu może wyglądać jak mętny roztwór. Nie ma to wpływu na wyniki. |
WYMAGANY SPRZĘT DO PRZETWARZANIA I ANALIZY
Analiza ręczna
- Eksplorator obrazu
- Uchwyt tablicy (opcjonalnie)
- Lab Rocker (kąt nachylenia 8°, wymagana prędkość 8 obr/min)
- Komora inkubacyjna (szer. x gł. x wys. – 35x25x2 cm)
- Oprogramowanie analityczne RAPTOR SERVER
- Komputer stacjonarny/Laptop
Wymagany sprzęt, którego nie zapewnia MADx:
- Woda demineralizowana
- Pipety i końcówki (100 µl i 100 – 1000 µl)
Automatyczna analiza:
- Urządzenie MAX (MAX 45k lub MAX 9k)
- Roztwór do mycia (REF 00-5003-01)
- Rozwiązanie zatrzymujące (REF 00-5007-01)
- Oprogramowanie analityczne RAPTOR SERVER
- Komputer stacjonarny/Laptop
Usługi serwisowe zgodnie z zaleceniami producenta.
OBSŁUGA TABLIC
Nie dotykaj powierzchni matrycy. Wszelkie wady powierzchni spowodowane przez tępe lub ostre przedmioty mogą zakłócać prawidłowy odczyt wyników. Nie pobieraj obrazów ALEX², dopóki matryca nie wyschnie całkowicie (sucho w temperaturze pokojowej).
OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI
- Zaleca się noszenie środków ochrony rąk i oczu oraz fartuchów laboratoryjnych i przestrzeganie dobrych praktyk laboratoryjnych podczas przygotowywania i obchodzenia się z odczynnikami i substancjamiamples.
- Zgodnie z dobrą praktyką laboratoryjną, cały materiał pochodzenia ludzkiego należy uznać za potencjalnie zakaźny i należy się z nim obchodzić z zachowaniem takich samych środków ostrożności jak materiał pacjentaamples.
- ALEX² SampRozcieńczalnik i roztwór myjący zawierają azydek sodu (<0.1%) jako środek konserwujący i należy obchodzić się z nimi ostrożnie. Karta charakterystyki bezpieczeństwa jest dostępna na żądanie.
- Roztwór (ALEX²) Stop zawiera kwas etylenodiaminotetraoctowy (EDTA)-Roztwór i należy obchodzić się z nim ostrożnie. Karta charakterystyki jest dostępna na żądanie.
- Tylko do diagnostyki in vitro. Nie do użytku wewnętrznego ani zewnętrznego u ludzi ani zwierząt.
- Z tego zestawu powinien korzystać wyłącznie personel przeszkolony w praktyce laboratoryjnej.
- Po otrzymaniu sprawdź elementy zestawu pod kątem uszkodzeń. Jeśli jeden z elementów jest uszkodzony (np. butelki buforowe), skontaktuj się z MADx (wsparcie@madx.com) lub lokalnego dystrybutora. Nie używaj uszkodzonych komponentów zestawu, ponieważ ich użycie może prowadzić do słabej wydajności zestawu.
- Nie używać odczynników po upływie terminu ważności.
- Nie mieszać odczynników z różnych partii.
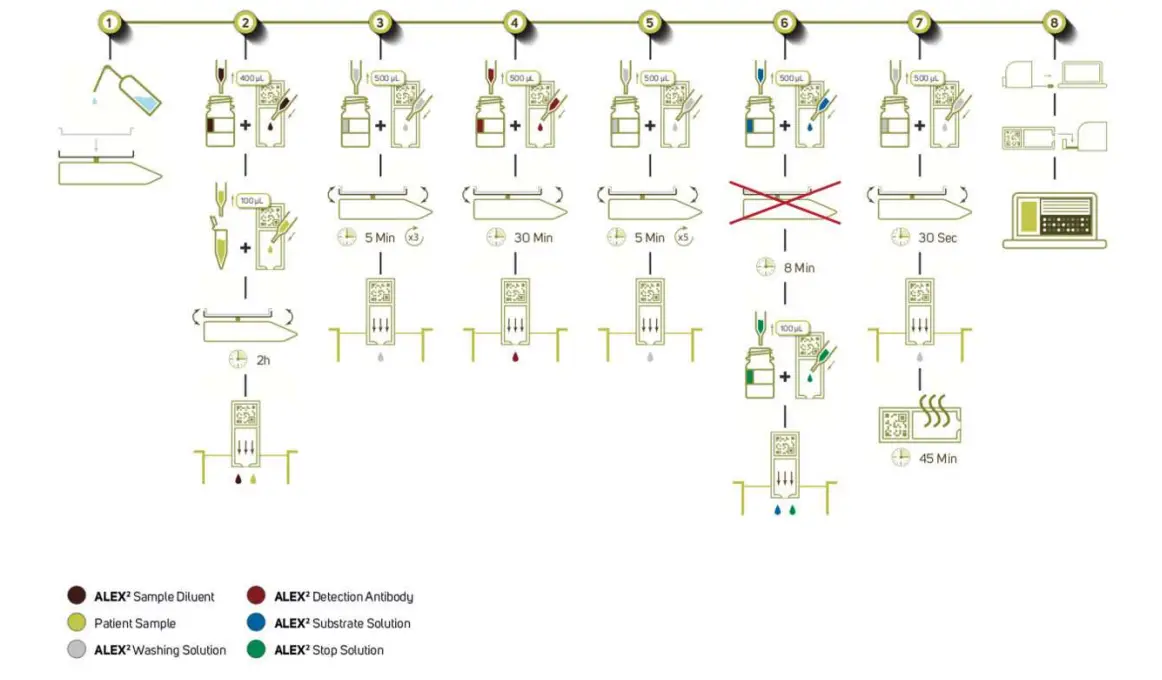
PROCEDURA ELISA
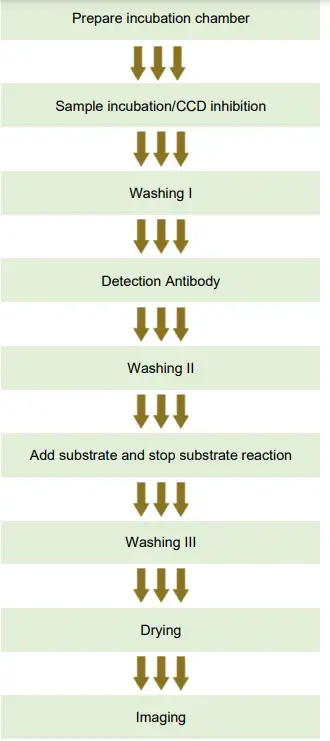
Przygotowanie
Przygotowanie samples: Surowica lub osocze (heparyna, cytrynian, bez EDTA)ampMożna stosować pliki z krwi włośniczkowej lub żylnej. Krew sampPliki można gromadzić przy użyciu standardowych procedur. Sklep samples w temperaturze 2–8°C przez okres do jednego tygodnia. Przechowywać surowicę i osoczeampprzechowywać w temperaturze -20°C w celu długotrwałego przechowywania. Wysyłka surowicy/osoczaampobowiązuje temperatura pokojowa. Zawsze zezwalaj na sampprzed użyciem należy uzyskać temperaturę pokojową.
Przygotowanie roztworu myjącego (tylko dla REF 02-5001-01 i REF 00-5003-01 w przypadku stosowania z urządzeniem MAX): Wlać zawartość 1 fiolki roztworu myjącego do pojemnika myjącego urządzenia. Napełnić wodą demineralizowaną do czerwonego znaku i ostrożnie wymieszać pojemnik kilka razy, nie wytwarzając piany. Otwarty odczynnik jest stabilny przez 6 miesięcy w temperaturze 2-8°C.
Komora inkubacyjna: Zamknij pokrywę na czas wykonywania wszystkich etapów testu, aby zapobiec spadkowi wilgotności.
Parametry of Procedura:
- 100 µl samplej + 400 µl ALEX² SampRozcieńczalnik
- 500 µl przeciwciała wykrywającego ALEX²
- 500 µl roztworu substratu ALEX²
- 100 µl (ALEX²) Roztwór zatrzymujący
- 4500 µl roztworu do mycia
Czas trwania testu wynosi około 3 godz. 30 min (bez suszenia przetworzonej macierzy).
Nie zaleca się przeprowadzania większej liczby testów niż można odpipetować w ciągu 8 min. Wszystkie inkubacje przeprowadza się w temperaturze pokojowej, 20-26°C.
Wszystkie odczynniki należy stosować w temperaturze pokojowej (20–26°C). Testu nie należy wykonywać w bezpośrednim świetle słonecznym.
Przygotuj komorę inkubacyjną
Otwórz komorę inkubacyjną i umieść ręczniki papierowe na dolnej części. Namocz ręczniki papierowe w wodzie demineralizowanej, aż nie będą widoczne żadne suche części ręczników papierowych.
Sampinkubacja/hamowanie CCD
Wyjmij potrzebną liczbę wkładów ALEX² i umieść je w uchwycie(ach) matrycy. Dodaj 400 μl ALEX² Sample Rozcieńczalnik do każdego wkładu. Dodaj 100 μl pacjenta sample do wkładów. Upewnij się, że powstały roztwór jest równomiernie rozprowadzony. Umieść wkłady w przygotowanej komorze inkubacyjnej i umieść komorę inkubacyjną z wkładami na kołysce laboratoryjnej tak, aby wkłady kołysały się wzdłuż dłuższego boku wkładu. Rozpocznij inkubację surowicy przy 8 obr./min przez 2 godziny. Zamknij komorę inkubacyjną przed uruchomieniem kołyski laboratoryjnej. Po 2 godzinach rozładuj samppliki do pojemnika zbiorczego. Ostrożnie wytrzyj kropelki z wkładu za pomocą papierowego ręcznika.
Unikaj dotykania powierzchni tablicy ręcznikiem papierowym! Unikaj przenoszenia lub krzyżowego zanieczyszczenia sampmiędzy poszczególnymi wkładami ALEX²!
Opcjonalny lub pozytywny Hom s LF (znacznik CCD): ze standardowym protokołem hamowania przeciwciał CCD (jak opisano w punkcie 2: samp(inkubacja/hamowanie CCD) wydajność hamowania CCD wynosi 85%. Jeśli wymagana jest wyższa wydajność hamowania, należy przygotować próbkę 1 mlampdo probówki dodać 400 μl ALEX² Sample Diluent i 100 μl surowicy. Inkubować przez 30 minut (bez wstrząsania), a następnie postępować zgodnie ze zwykłą procedurą badania.
Notatka: Dodatkowy etap hamowania CCD prowadzi w wielu przypadkach do wskaźnika hamowania przeciwciał CCD przekraczającego 95%.
1a. Mycie I
Dodaj 500 μl roztworu do mycia do każdego wkładu i inkubuj na laboratoryjnym kołyskowym urządzeniu (przy 8 obr./min) przez 5 minut. Wylej roztwór do mycia do pojemnika zbiorczego i energicznie uderz wkłady o stos suchych ręczników papierowych. Ostrożnie wytrzyj pozostałe krople z wkładów za pomocą ręcznika papierowego.
Powtórz ten krok jeszcze 2 razy.
Dodaj przeciwciało wykrywające
Dodać 500 µl przeciwciała wykrywającego ALEX² do każdego wkładu.
Upewnij się, że cała powierzchnia matrycy jest pokryta roztworem przeciwciał wykrywających ALEX².
Umieść wkłady w komorze inkubacyjnej na kołysce laboratoryjnej i inkubuj przy 8 obr./min przez 30 minut. Wylej roztwór przeciwciał wykrywających do pojemnika zbiorczego i energicznie uderz wkłady o stos suchych ręczników papierowych. Ostrożnie wytrzyj pozostałe krople z wkładów za pomocą ręcznika papierowego.
2a. Mycie II
Dodaj 500 μl roztworu do mycia do każdego wkładu i inkubuj na laboratoryjnym urządzeniu kołyskowym przy 8 obr./min przez 5 minut. Wylej roztwór do mycia do pojemnika zbiorczego i energicznie uderz wkłady o stos suchych ręczników papierowych. Ostrożnie wytrzyj pozostałe krople z wkładów za pomocą ręcznika papierowego.
Powtórz ten krok jeszcze 4 razy.
3+4. Dodaj roztwór substratu ALEX² i zatrzymaj reakcję substratu
Dodaj 500 μl roztworu substratu ALEX² do każdego wkładu. Rozpocznij odliczanie od napełnienia pierwszego wkładu i kontynuuj napełnianie pozostałych wkładów. Upewnij się, że cała powierzchnia matrycy jest pokryta roztworem substratu i inkubuj matryce dokładnie przez 8 minut bez potrząsania (kołyska laboratoryjna przy 0 obr./min i w pozycji poziomej).
Dokładnie po 8 minutach dodaj 100 μl roztworu zatrzymującego (ALEX²) do wszystkich wkładów, zaczynając od pierwszego wkładu, aby upewnić się, że wszystkie macierze są inkubowane przez ten sam czas z roztworem substratu ALEX². Ostrożnie wymieszaj, aby równomiernie rozprowadzić roztwór zatrzymujący (ALEX²) w wkładach macierzy, po tym jak roztwór zatrzymujący (ALEX²) został odpipetowany na wszystkie macierze. Następnie usuń roztwór substratu/stopu (ALEX²) z wkładów i energicznie uderz wkładami o stos suchych ręczników papierowych. Ostrożnie wytrzyj wszelkie pozostałe krople z wkładów za pomocą ręcznika papierowego.
Podgrzewacz Lab Rocker NIE MOŻE SIĘ TRZĄSAĆ podczas inkubacji podłoża!
4a. Mycie III
Dodaj 500 μl roztworu do mycia do każdego wkładu i inkubuj na laboratoryjnym urządzeniu kołyskowym przy 8 obr./min przez 30 sekund. Wylej roztwór do mycia do pojemnika zbiorczego i energicznie uderz wkłady o stos suchych ręczników papierowych. Ostrożnie wytrzyj wszelkie pozostałe krople z wkładów za pomocą ręcznika papierowego.
Analiza obrazu
Po zakończeniu procedury testowej należy wysuszyć macierze na powietrzu w temperaturze pokojowej, aż do całkowitego wyschnięcia (może to potrwać do 45 minut).
Całkowite wysuszenie jest niezbędne dla czułości testu. Tylko całkowicie wysuszone tablice zapewniają optymalny stosunek sygnału do szumu.
Na koniec wysuszone macierze są skanowane za pomocą ImageXplorer lub urządzenia MAX i analizowane za pomocą oprogramowania RAPTOR SERVER Analysis (szczegóły w podręczniku oprogramowania RAPTOR SERVER). Oprogramowanie RAPTOR SERVER Analysis jest weryfikowane wyłącznie w połączeniu z instrumentem ImageXplorer i urządzeniami MAX, dlatego MADx nie bierze żadnej odpowiedzialności za wyniki uzyskane za pomocą innych urządzeń do przechwytywania obrazu (takich jak skanery).
Kalibracja testu
Główna krzywa kalibracji ALEX² została ustalona poprzez testowanie referencyjne preparatów surowicy ze swoistym IgE przeciwko różnym antygenom obejmującym zamierzony zakres pomiarowy. Parametry kalibracji specyficzne dla partii są dostarczane przez oprogramowanie analityczne RAPTOR SERVER. Wyniki testu sIgE ALEX² są wyrażone jako kUA/l. Całkowite wyniki IgE są półilościowe i obliczane na podstawie pomiaru anty-IgE ze współczynnikami kalibracji specyficznymi dla partii, które są dostarczane przez oprogramowanie analityczne RAPTOR SERVER i wybierane zgodnie z kodami QR specyficznymi dla partii.
Parametry krzywej dla każdej partii są dostosowywane przez wewnętrzny system testowania referencyjnego, w odniesieniu do preparatów surowicy testowanych na ImmunoCAP (Thermo Fisher Scientific) pod kątem swoistego IgE przeciwko kilku alergenom. Wyniki ALEX² są zatem pośrednio śledzone w odniesieniu do preparatu referencyjnego WHO 11/234 pod kątem całkowitego IgE.
Systematyczne zmiany poziomów sygnału między partiami są normalizowane przez heterologiczną kalibrację względem krzywej odniesienia IgE. Współczynnik korekcji jest używany do systematycznego dostosowywania odchyleń pomiaru specyficznych dla partii.
Zakres pomiarowy
Specyficzne IgE: 0.3-50 kUA/l ilościowo
Całkowite IgE: 20-2500 kU/l półilościowo
KONTROLA JAKOŚCI
Prowadzenie dokumentacji dla każdego testu
Zgodnie z dobrą praktyką laboratoryjną zaleca się zapisywanie numerów partii wszystkich użytych odczynników.
Próbki kontrolne
Zgodnie z dobrą praktyką laboratoryjną zaleca się, aby kontrola jakości samples są zawarte w zdefiniowanych przedziałach. Wartości referencyjne dla niektórych komercyjnie dostępnych surowic kontrolnych mogą być dostarczone przez MADx na żądanie.
ANALIZA DANYCH
Do analizy obrazu przetworzonych tablic należy użyć urządzenia ImageXplorer lub MAX. Obrazy ALEX² są automatycznie analizowane przy użyciu oprogramowania RAPTOR SERVER Analysis Software, a następnie generowany jest raport podsumowujący wyniki dla użytkownika.
WYNIKI
ALEX² to ilościowy test ELISA na swoiste IgE i półilościowa metoda na całkowite IgE. Przeciwciała IgE swoiste dla alergenu są wyrażone jako jednostki odpowiedzi IgE (kUA/l), a wyniki całkowitego IgE jako kU/l. Oprogramowanie analityczne RAPTOR SERVER automatycznie oblicza i raportuje wyniki sIgE (ilościowo) i wyniki tIgE (półilościowo).
OGRANICZENIA PROCEDURY
Ostateczna diagnoza kliniczna powinna zostać postawiona wyłącznie na podstawie wszystkich dostępnych wyników badań klinicznych, dokonanych przez personel medyczny, a nie na podstawie wyników pojedynczej metody diagnostycznej.
W pewnych obszarach zastosowań (np. alergia pokarmowa) krążące przeciwciała IgE mogą pozostać niewykrywalne, pomimo występowania klinicznych objawów alergii pokarmowej na konkretny alergen. Wynika to z faktu, że przeciwciała te mogą być specyficzne dla alergenów modyfikowanych podczas przetwarzania przemysłowego, gotowania lub trawienia, a zatem nie występują w oryginalnej żywności, na którą badany jest pacjent.
Ujemne wyniki badań na jad wskazują jedynie na niewykrywalny poziom przeciwciał IgE specyficznych dla jadu (np. z powodu długotrwałego braku narażenia) i nie wykluczają istnienia klinicznej nadwrażliwości na jad owadów.
U dzieci, zwłaszcza do 2. roku życia, normalny zakres tIgE jest niższy niż u nastolatków i dorosłych [7]. Dlatego należy się spodziewać, że u większej części dzieci poniżej 2. roku życia całkowity poziom IgE będzie niższy od określonego limitu wykrywalności. Ograniczenie to nie dotyczy pomiaru swoistego IgE.
OCZEKIWANE WARTOŚCI
Ścisły związek między poziomem przeciwciał IgE swoistych dla alergenu a chorobą alergiczną jest dobrze znany i dokładnie opisany w literaturze [1]. Każdy uczulony pacjent będzie wykazywał indywidualną pro IgEfile przy badaniu z ALEX². Odpowiedź IgE z samples od zdrowych osób bez alergii będą poniżej 0.3 kUA/l dla pojedynczych alergenów cząsteczkowych i dla ekstraktów alergenów, gdy testowane są za pomocą ALEX². Obszar odniesienia dla całkowitego IgE u osób dorosłych wynosi < 100 kU/l. Dobra praktyka laboratoryjna zaleca, aby każde laboratorium ustaliło własny zakres oczekiwanych wartości.
CHARAKTERYSTYKA WYDAJNOŚCIOWA
Charakterystykę wydajnościową oraz podsumowanie bezpieczeństwa i wydajności można znaleźć na stronie MADx webstrona: https://www.madx.com/extras.
GWARANCJA
Dane dotyczące wydajności uzyskano przy użyciu procedury opisanej w niniejszej Instrukcji użytkowania. Wszelkie zmiany lub modyfikacje procedury mogą mieć wpływ na wyniki, a MacroArray Diagnostics zrzeka się wszelkich wyrażonych gwarancji (w tym domniemanej gwarancji przydatności handlowej i przydatności do użytku) w takim przypadku. W związku z tym MacroArray Diagnostics i jego lokalni dystrybutorzy nie ponoszą odpowiedzialności za szkody pośrednie lub następcze w takim przypadku.
SKRÓTY
| ALEKSA | Alergia Xplorer |
| CCD | Krzyżowo reaktywne determinanty węglowodanowe |
| EDTA | Kwas etylenodiaminotetraoctowy |
| ELISA | Test immunoenzymatyczny |
| IgE | Immunoglobulina E |
| IVD | Diagnostyka in vitro |
| kU/l | Kilojednostki na litr |
| kUA/l | Kilogramy jednostek IgE swoistych dla alergenu na litr |
| MADx | Diagnostyka makromacierzy |
| ODNOŚNIK | Numer referencyjny |
| obr./min | Rund na minutę |
| sIge | Alergenowo swoiste IgE |
| tIge | Całkowite IgE |
| ul | Mikrolitr |
LISTA ALERGENÓW ALEX²
Wyciągi alergenów: Aca m, Aca s, Ach d, Ail a, All c, All s, Ama r, Amb a, Ana o, Api m, Art v, Ave s, Ber e, Bos d meat, Bos d milk, Bro p, Cam d, Can f ♂ mocz, Can s, Cap a, Cap h epithelia, Cap h milk, Car c, Car i, Car p, Che a, Che q, Chi spp., Cic a, Cit s, Cla h, Clu h, Cor a pollen, Cuc p, Cup s, Cyn d, Dau c, Dol spp., Equ c milk, Equ c meat, Fag e, Fic b, Fic c, Fra e, Gad m, Gal d meat, Gal d white, Gal d yolk, Hel a, Hom g, Hor v, Jug r, Jun a, Len c, Lit s, Loc m, Lol spp., Lup a, Mac i, Man i, Mel g, Mor r, Mus a, Myt e, Ori v, Ory mięso, Ory s, Ost e, Ovi a epithelia, Ovi a meat, Ovi a milk, Pan b, Pan m, Pap s, Par j, Pas n, Pec spp., Pen ch, Per a, Pers a, Pet c, Pha v, Phr c, Pim a, Pis s, Pla l, Pol d, Pop n, Pru av, Pru du, Pyr c, Raj c, Rat n, Rud spp., Sac c, Sal k, Sal s, Sco s, Sec c flour, Sec c pollen, Ses i, Sin, Sol spp., Sola l, Sol t, Sus d epithel, Sus d meat, Ten m, Thu a, Tri fo, Tri s, Tyrp, Ulm c, Urt d, Vac m, Ves v, Zea mąka
Oczyszczone składniki naturalne: nAct d 1, nApi m 1, nara h 1, naAra h 3, nBos d 4, nBos d 5, nBos d 6, nBos d 8, nCan f 3, nCor a 9, nCor a 11, nCup a 1, nCry j 1, nEqu c 3, nFage 2, nGad m 1, nGad m 2 + 3, nGal d 2, nGal d 3, nGal d 4, nGal d 5, nGly m 5, nGly m 6, nJug r 4, nMac i 2S Albumina, nOle e 7 (RUO), nPap s 2S Albumina, nPis v 3, nPla a 2, nTri a aA_TI
Składniki rekombinowane: rAct d 10, rAct d 2, rAct d 5, rAln g 1, rAln g 4, rAlt a 1, rAlt a 6, ramb a 1, ramb a 4, rAna o 2, rAna o 3, rAni s 1, rAni s 3, rApi g 1, rApi g 2, rApi g 6, rApi m 10, rAra h 2, rAra h 6, rAra h 8, rAra h 9, rAra h 15, rArg r 1, rArt v 1, rArt v 3, zgrzyt f 1, zgrzyt f 3, zgrzyt f 4, zgrzyt f 6, rBer e 1, rBet v 1, rBet v 2, rBet v 6, rBla g 1, rBla g 2, rBla g 4, rBla g 5, rBla g 9, rBlo t 10, rBlo t 21, rBlo t 5, rBos d 2, rCan f 1, rCan f 2, rCan f 4, rCan f 6, rCan f Fel d 1 jak, rCan s 3, rCav p 1, rChe a 1, rCla h 8, rClu h 1, rCor a 1.0103, rCor a 1.0401, rCor a 8, rCor a 12 (RUO), rCor a 14, rCra c 6, , rCuc m 2, rCyn d 1, rCyp c 1, rDau c 1, rDer f 1, rDer f 2, rDer p 1, rDer p 10, rDer p 11, rDer p 2, rDer p 20, rDer p 21, rDer p 23, rDer p 5, rDer p 7, rEqu c 1, rEqu c 4, rFag s 1, rFel d 1, rFel d 2, rFel d 4, rFel d 7, rFra a 1 + 3, rFra e 1, rGal d 1, rGly d 2, rGly m 4, rGly m 8, rHev b 1, rHev b 3, rHev b 5, rHev b 6.02, rHev b 8, rHev b 11, rHom s LF, rJug r 1, rJug r 2, rJug r 3, rJug r 6, rLep d 2, rLol p 1, rMal d 1, rMal d 3, rMala s 11, rMala s 5, rMala s 6, rMal d 2, rMer a 1, rMes a 1 (RUO), rMus m 1, rola 1, rola 9, rOry c 1, rOry c 2, rOry c 3, rPar j 2, rPen m 1, rPen m 2, rPen m 3, rPen m 4, rPer a 7, rPhl p 1, rPhl p 12, rPhl p 2, rPhl p 5.0101 , rPhl str 6, rPhl str 7, rPhod 2, rPhod s 1, rPis v 1, rPis v 2, rPis v 4 (RUO), rPla a 1, rPla a 3, rPla l 1, rPol d 5, rPru p 3, rPru p 7 (RUO), rRaj c Parwalbumina, rSal k 1, rSal s 1, rSco s 1, rSes i 1, rSin a 1, rSola l 6 , rSus d 1, rThu a 1, rTri a 14, rTri a 19, rTyr p 2, rVes v 1, rVes v 5, rVit v 1, rXip g 1, rZea m 14
REFERENCJE
- Hamilton, RG. (2008). Ocena ludzkich chorób alergicznych. Immunologia kliniczna. 1471-1484. 10.1016/B978-0-323-04404-2.10100-9.
- Harwanegg C, Laffer S, Hiller R, Mueller MW, Kraft D, Spitzauer S, Valenta R. Mikromacierzowe alergeny rekombinowane do diagnostyki alergii. Clin Exp Allergy. 2003 styczeń;33(1):7-13. doi: 10.1046/j.1365-2222.2003.01550.x. PMID: 12534543.
- Hiller R, Laffer S, Harwanegg C, Huber M, Schmidt WM, Twardosz A, Barletta B, Becker WM, Blaser K, Breiteneder H, Chapman M, Crameri R, Duchêne M, Ferreira F, Fiebig H, Hoffmann-Sommergruber K, King TP, Kleber-Janke T, Kurup VP, Lehrer SB, Lidholm J, Müller U, Pini C, Reese G, Scheiner O, Scheynius A, Shen HD, Spitzauer S, Suck R, Swoboda I, Thomas W, Tinghino R, Van Hage-Hamsten M, Virtanen T, Kraft D, Müller MW, Valenta R. Mikromacierzowe cząsteczki alergenów: diagnostyczni strażnicy w leczeniu alergii. FASEB J. 2002 marzec;16(3):414-6. doi: 10.1096/fj.01-0711fje. Epub 2002 styczeń 14. PMID: 11790727
- Ferrer M, Sanz ML, Sastre J, Bartra J, del Cuvillo A, Montoro J, Jáuregui I, Dávila I, Mullol J, Valero A. Diagnostyka molekularna w alergologii: zastosowanie techniki mikromacierzy. J Investig Allergol Clin Immunol. 2009;19 Suppl 1:19-24. PMID: 19476050.
- Ott H, Fölster-Holst R, Merk HF, Baron JM. Mikromacierze alergenów: nowe narzędzie do profilowania IgE o wysokiej rozdzielczości u dorosłych z atopowym zapaleniem skóry. Eur J Dermatol. 2010 styczeń-luty;20(1):54-
61. doi: 10.1684/ejd.2010.0810. EPUB 2009 października 2 r. PMID: 19801343. - Sastre J. Diagnostyka molekularna w alergii. Clin Exp Allergy. 2010 paź;40(10):1442-60. doi: 10.1111/j.1365-2222.2010.03585.x. Epub 2010 sierpnia 2. PMID: 20682003.
- Martins TB, Bandhauer ME, Bunker AM, Roberts WL, Hill HR. Nowe przedziały referencyjne dla dzieci i dorosłych dla całkowitego IgE. J Allergy Clin Immunol. 2014 luty;133(2):589-91.
Szczegółowe informacje na temat przeprowadzonych badań analitycznych i klinicznych można znaleźć w charakterystyce wydajności na stronie https://www.madx.com/extras.
ZMIENIAĆ HISTORIĘ
| Wersja | Opis | Zastępuje |
| 11 | nGal d1 zmieniono na rGal d1; URL zaktualizowano do madx.com; CE uzupełniono o numer Jednostki Notyfikowanej; dodano historię zmian | 10 |

© Copyright by MacroArray Diagnostics
Diagnostyka MacroArray (MADx)
Lemböckgasse 59, Top 4
1230 Wiedeń, Austria
+43 (0)1 865 2573
www.madx.com
Numer wersji: 02-IFU-01-EN-11 Wydano: 09-2024
Szybka porada
Diagnostyka makromacierzy
Lemböckgasse 59, Top 4
1230 Wiedeń
madx.com
CRN 448974 gr
Dokumenty / Zasoby
 |
MacroArray ALLERGY XPLORER Diagnostyka MacroArray [plik PDF] Instrukcje 91201229202JQ, 02-2001-01, 02-5001-01, ALLERGY XPLORER Diagnostyka makromacierzy, ALLERGY XPLORER, Diagnostyka makromacierzy, Diagnostyka matryc, Diagnostyka |




