Sistema automatizzato di somministrazione di insulina Omnipod
Specifiche del prodotto
- Nome del prodotto: Sistema automatico di somministrazione di insulina senza tubi
- Tipo: Dispositivo medico
- Caratteristiche: Senza camera d'aria, sul corpo, obiettivi glicemici personalizzabili
- Fascia d'età: bambini molto piccoli con diabete di tipo 1
- Durata: fase di terapia standard di 14 giorni seguita da una fase AID di 3 mesi con il sistema Omnipod 5
Informazioni sulla sicurezza
- Obiettivo clinico: per valutare la sicurezza e l'efficacia del sistema di somministrazione automatizzata di insulina (AID) Omnipod® 5, il primo sistema AID senza tubi, da indossare sul corpo, con obiettivi glicemici personalizzabili, nei bambini molto piccoli affetti da diabete di tipo 1.
- Endpoint primari:
- HbA1c alla fine della fase AID rispetto al basale
- Tempo nell'intervallo 3.9–10.0 mmol/L durante la fase AID rispetto alla fase di terapia standard (ST)
- Tassi di incidenza di ipoglicemia grave o chetoacidosi diabetica (DKA)
- Endpoint secondari includeva la percentuale di tempo con livelli di glucosio <3.9 mmol/L e >10.0 mmol/L durante la fase AID rispetto alla fase ST.
Istruzioni per l'uso
Progettazione dello studio
- Studio ambulatoriale multicentrico a braccio singolo:
- Fase ST di 14 giorni
- Fase AID di 3 mesi con sistema Omnipod 5
- Nessun requisito di peso corporeo minimo o dose giornaliera totale di insulina
Partecipanti allo studio
- 80 bambini con diabete di tipo 1: età compresa tra 2.0 e 5.9 anni, con consenso informato del caregiver
- HbA1c <10% (86 mmol/mol) allo screening
- Non è richiesto l'uso precedente della pompa o del CGM
- Criteri di esclusione: storia di DKA o ipoglicemia grave negli ultimi 6 mesi
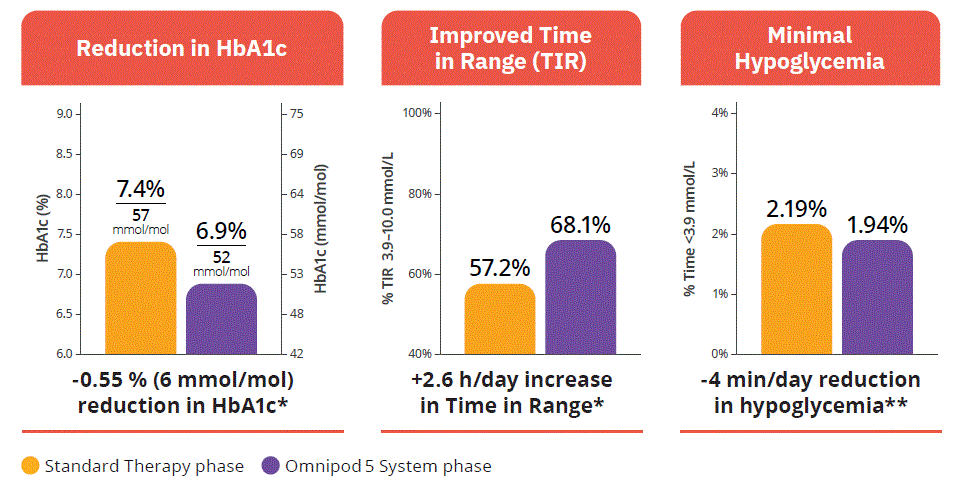
- p<0.0001.
- p=0.02.
- Per l'endpoint primario dell'HbA1c sono stati utilizzati i dati basali e di follow-up. I dati sono mostrati per la fase di terapia standard e la fase di AIDS. I dati sono mostrati come mediana per il tempo <3.9 mmol/L e media per tutti gli altri esiti.
- Non si sono verificati episodi di ipoglicemia grave o di chetoacidosi diabetica nella fase AID.
Caratteristiche
Punti salienti dello studio
- Rispetto alla fase ST, il sistema Omnipod 5 ha abbassato l'HbA1c, aumentato il TIR e ridotto l'ipoglicemia nei bambini molto piccoli con diabete di tipo 1
- Tempo nel range durante la notte (00:00 – 06:00 h) aumentato dal 58.2% (fase ST) all'81.0% (fase Omnipod 5)
- Non si sono verificati episodi di ipoglicemia grave o DKA nella fase AID
- La percentuale di bambini che hanno raggiunto gli obiettivi di consenso per HbA1c, <7.0% (53 mmol/mol), è aumentata dal 31% con la terapia abituale al 54% dopo aver utilizzato il sistema Omnipod 5
- La percentuale di bambini che raggiungono gli obiettivi per >70% di tempo nell'intervallo è aumentata di 2.5 volte, dal 17% con la terapia abituale al 44% dopo aver utilizzato il sistema Omnipod 5
- Il tempo mediano in modalità automatica durante la fase del sistema Omnipod 5 è stato del 97.8%
- Il sistema Omnipod 5 può essere utilizzato in modo sicuro ed efficace nei bambini molto piccoli affetti da diabete di tipo 1

Questo riepilogo è stato fornito nell'ambito dell'Omnipod Academy, un servizio formativo offerto da Insulet ai professionisti sanitari.
Descrizione del prodotto
Riferimenti 1. Adattato da; Sherr JL, et al. Sicurezza e risultati glicemici con un sistema di somministrazione automatizzata di insulina senza tubi in bambini molto piccoli con diabete di tipo 1: uno studio clinico multicentrico a braccio singolo
Prova. Diabetes Care 2022; 45:1907-1910.
- In uno studio clinico della durata di 3 mesi, sono stati segnalati 0 casi di ipoglicemia grave e 0 casi di chetoacidosi diabetica (DKA) nei bambini durante l'uso del sistema Omnipod 5.
- Il sistema automatizzato di somministrazione di insulina Omnipod 5 è un sistema di somministrazione di insulina monoormonale progettato per somministrare insulina U-100 per via sottocutanea per la gestione del diabete di tipo 1 in soggetti dai 2 anni in su che necessitano di insulina. Il sistema Omnipod 5 è destinato all'uso su un singolo paziente.
- Il sistema Omnipod 5 è progettato per funzionare come un sistema di somministrazione automatica di insulina se utilizzato con sistemi di monitoraggio continuo del glucosio (CGM) compatibili. In modalità automatica, il sistema Omnipod 5 è progettato per aiutare le persone con diabete di tipo 1 a raggiungere gli obiettivi glicemici stabiliti dai loro operatori sanitari. È progettato per modulare (aumentare, diminuire o sospendere) l'erogazione di insulina entro valori soglia predefiniti, utilizzando i valori CGM correnti e previsti per mantenere la glicemia a livelli target variabili, riducendo così la variabilità della glicemia. Questa riduzione della variabilità ha lo scopo di ridurre la frequenza, la gravità e la durata sia dell'iperglicemia che dell'ipoglicemia.
- Il sistema Omnipod 5 può funzionare anche in modalità manuale, erogando insulina a velocità preimpostate o regolate manualmente.
Il sistema Omnipod 5 è indicato per l'uso con insulina NovoLog®/NovoRapid®, Humalog®/Liprolog®, Trurapi®/Truvelog®/Insulin aspart Sanofi®, Kirsty® e Admelog®/Insulin lispro Sanofi U-100. Avvertenze:
- La tecnologia SmartAdjust™ NON deve essere utilizzata da bambini di età inferiore a 2 anni.
- La tecnologia SmartAdjust™ NON deve essere utilizzata da persone che necessitano di meno di 5 unità di insulina al giorno, poiché la sicurezza della tecnologia non è stata valutata in questa popolazione.
- Il sistema Omnipod 5 NON è raccomandato per le persone che non sono in grado di monitorare la glicemia come raccomandato dal proprio medico curante, non sono in grado di mantenere i contatti con il proprio medico curante, non sono in grado di utilizzare il sistema Omnipod 5 secondo le istruzioni, stanno assumendo idrossiurea poiché potrebbe portare a valori CGM falsamente elevati e causare una sovradosaggio di insulina che può portare a grave ipoglicemia, e NON hanno un udito e/o una vista adeguati per consentire il riconoscimento di tutte le funzioni del sistema Omnipod 5, inclusi avvisi, allarmi e promemoria. I componenti del dispositivo, tra cui il Pod, il trasmettitore CGM e il sensore CGM, devono essere rimossi prima di sottoporsi a risonanza magnetica (RM), tomografia computerizzata (TC) o diatermia. Inoltre, il controller e lo smartphone devono essere posizionati all'esterno della sala operatoria. L'esposizione a risonanza magnetica, TC o diatermia può danneggiare i componenti.
- Per un elenco completo di indicazioni, controindicazioni, avvertenze, precauzioni e istruzioni, consultare il Manuale d'uso del sistema automatizzato di somministrazione di insulina Omnipod 5. Le guide sono disponibili chiamandoci al numero 1-855-POD-INFO (1-Numero di telefono: 855-763-4636) o visitando il nostro websito a omnipod.com
- ©2025 Insulet Corporation. Omnipod e il logo Omnipod sono marchi commerciali o marchi registrati di Insulet Corporation negli Stati Uniti d'America e in altre giurisdizioni. Tutti i diritti riservati. Tutti gli altri marchi commerciali sono di proprietà dei rispettivi titolari. L'uso di marchi commerciali di terze parti non costituisce un'approvazione né implica una relazione o altra affiliazione.
- Insulet Corporation, 1540 Cornwall Rd, Suite 201, Oakville, ON L6J 7W5. INS-OHS-12-2024-00217 V1.0
Domande frequenti
- D: Chi dovrebbe utilizzare questo sistema automatizzato di somministrazione di insulina senza tubi?
- R: Questo sistema è progettato per bambini molto piccoli affetti da diabete di tipo 1, sotto la supervisione di operatori sanitari.
- D: Quali sono gli obiettivi principali dell'utilizzo di questo sistema?
- R: Gli endpoint primari includono la valutazione dei livelli di HbA1c alla fine della fase AID rispetto al basale e il confronto dei tassi di incidenza di ipoglicemia grave o chetoacidosi diabetica con la terapia standard.
- D: Quanto dura il periodo di studio per l'utilizzo di questo dispositivo?
- R: Lo studio prevede una fase di terapia standard di 14 giorni seguita da una fase AID di 3 mesi con il sistema Omnipod 5.
Documenti / Risorse
 |
Sistema automatizzato di somministrazione di insulina Omnipod [pdf] Manuale del proprietario Sistema di somministrazione automatizzata di insulina, sistema di somministrazione di insulina, sistema di somministrazione |
