Système automatisé d'administration d'insuline Omnipod
Spécifications du produit
- Nom du produit : Système automatisé d'administration d'insuline sans tube
- Type : Dispositif médical
- Caractéristiques : Sans chambre à air, sur le corps, objectifs glycémiques personnalisables
- Tranche d'âge : Très jeunes enfants atteints de diabète de type 1
- Durée : Phase de thérapie standard de 14 jours suivie d'une phase AID de 3 mois avec le système Omnipod 5
Consignes de sécurité
- Objectif clinique : pour évaluer la sécurité et l'efficacité du système d'administration automatisée d'insuline (AID) Omnipod® 5, le premier système AID sans tube, sur le corps, avec des cibles glycémiques personnalisables, chez les très jeunes enfants atteints de diabète de type 1.
- Critères d'évaluation principaux :
- HbA1c à la fin de la phase AID par rapport à la valeur initiale
- Temps dans la plage de 3.9 à 10.0 mmol/L pendant la phase AID par rapport à la phase de traitement standard (ST)
- Taux d'incidence de l'hypoglycémie sévère ou de l'acidocétose diabétique (ACD)
- Critères d'évaluation secondaires inclus le pourcentage de temps avec des niveaux de glucose < 3.9 mmol/L et > 10.0 mmol/L pendant la phase AID par rapport à la phase ST.
Mode d'emploi
Conception de l'étude
- Étude à un seul bras, multicentrique, ambulatoire :
- Phase ST de 14 jours
- Phase AID de 3 mois avec le système Omnipod 5
- Aucune exigence de poids corporel minimum ou de dose quotidienne totale d'insuline
Participants à l'étude
- 80 enfants atteints de diabète de type 1 : âgés de 2.0 à 5.9 ans, avec le consentement éclairé du soignant
- HbA1c < 10 % (86 mmol/mol) au dépistage
- L'utilisation préalable d'une pompe ou d'un CGM n'est pas requise
- Critères d'exclusion : antécédents d'acidocétose diabétique ou d'hypoglycémie sévère au cours des 6 derniers mois
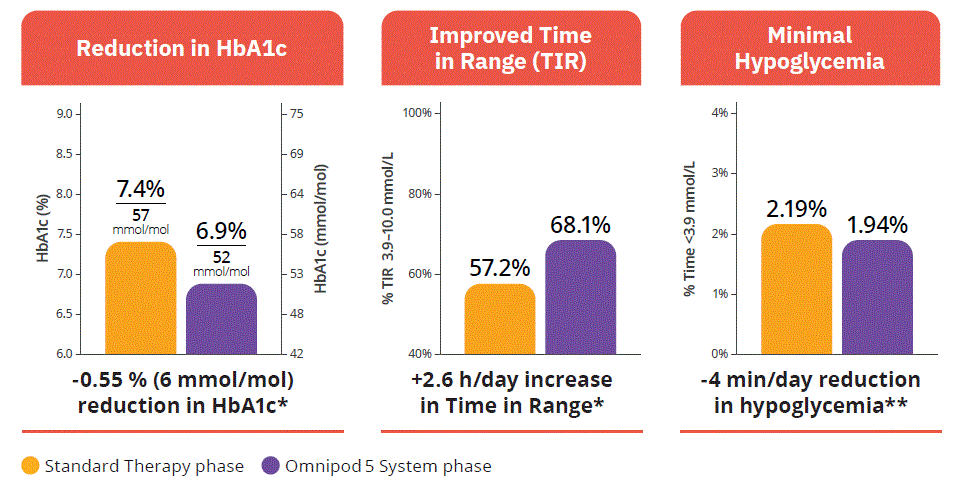
- p<0.0001.
- p=0.02.
- Les données initiales et de suivi ont été utilisées pour le critère d'évaluation principal de l'HbA1c. Les données sont présentées pour la phase de traitement standard et la phase d'AID. Les données sont présentées comme médianes pour une durée < 3.9 mmol/L et moyennes pour tous les autres critères.
- Il n’y a eu aucun épisode d’hypoglycémie sévère ou d’acidocétose diabétique au cours de la phase AID.
Caractéristiques
Points saillants de l'étude
- Par rapport à la phase ST, le système Omnipod 5 a abaissé l'HbA1c, augmenté le TIR et réduit l'hypoglycémie chez les très jeunes enfants atteints de diabète de type 1
- Le temps passé à portée pendant la nuit (00:00 – 06:00 h) est passé de 58.2 % (phase ST) à 81.0 % (phase Omnipod 5)
- Il n'y a eu aucun épisode d'hypoglycémie sévère ou d'ACD dans la phase AID
- La proportion d'enfants atteignant les objectifs consensuels pour l'HbA1c, < 7.0 % (53 mmol/mol), est passée de 31 % avec le traitement habituel à 54 % après l'utilisation du système Omnipod 5.
- La proportion d'enfants atteignant les objectifs pendant plus de 70 % du temps dans la plage a augmenté de 2.5 fois, passant de 17 % avec le traitement habituel à 44 % après l'utilisation du système Omnipod 5.
- Le temps médian en mode automatisé pendant la phase du système Omnipod 5 était de 97.8 %
- Le système Omnipod 5 peut être utilisé en toute sécurité et efficacement chez les très jeunes enfants atteints de diabète de type 1

Ce résumé a été fourni dans le cadre de l'Omnipod Academy, un service éducatif fourni aux professionnels de la santé par Insulet.
Description du produit
Références 1. Adapté de ; Sherr JL, et al. Sécurité et résultats glycémiques avec un système automatisé d'administration d'insuline sans tube chez les très jeunes enfants atteints de diabète de type 1 : une étude clinique multicentrique à un seul bras
Essai. Soins du diabète 2022; 45:1907-1910.
- Dans une étude clinique de 3 mois, 0 cas d’hypoglycémie sévère et 0 cas d’acidocétose diabétique (ACD) ont été signalés chez les enfants lors de l’utilisation du système Omnipod 5.
- Le système d'administration automatisée d'insuline Omnipod 5 est un système d'administration d'insuline monohormonale conçu pour administrer de l'insuline U-100 par voie sous-cutanée pour la prise en charge du diabète de type 1 chez les personnes de 2 ans et plus nécessitant de l'insuline. Le système Omnipod 5 est destiné à un usage unique.
- Le système Omnipod 5 est conçu pour fonctionner comme un système automatisé d'administration d'insuline lorsqu'il est utilisé avec des glucomètres en continu (CGM) compatibles. En mode automatisé, le système Omnipod 5 est conçu pour aider les personnes atteintes de diabète de type 1 à atteindre les objectifs glycémiques fixés par leurs professionnels de santé. Il est conçu pour moduler (augmenter, diminuer ou interrompre) l'administration d'insuline afin de respecter des seuils prédéfinis, en utilisant les valeurs actuelles et prévues du CGM, afin de maintenir la glycémie à des niveaux cibles variables, réduisant ainsi la variabilité glycémique. Cette réduction de la variabilité vise à réduire la fréquence, la gravité et la durée des hyperglycémies et des hypoglycémies.
- Le système Omnipod 5 peut également fonctionner en mode manuel qui délivre de l'insuline à des débits définis ou ajustés manuellement.
Le système Omnipod 5 est indiqué pour une utilisation avec les insulines NovoLog®/NovoRapid®, Humalog®/Liprolog®, Trurapi®/Truvelog®/Insuline asparte Sanofi®, Kirsty® et Admelog®/Insuline lispro Sanofi U-100. Avertissements :
- La technologie SmartAdjust™ ne doit PAS être utilisée par des personnes de moins de 2 ans.
- La technologie SmartAdjust™ ne doit PAS être utilisée par les personnes qui ont besoin de moins de 5 unités d’insuline par jour, car la sécurité de la technologie n’a pas été évaluée dans cette population.
- Le système Omnipod 5 n'est PAS recommandé aux personnes qui ne peuvent pas surveiller leur glycémie comme recommandé par leur professionnel de santé, qui ne peuvent pas maintenir le contact avec ce dernier, qui ne peuvent pas utiliser le système Omnipod 5 conformément aux instructions, qui prennent de l'hydroxyurée, car cela pourrait fausser les valeurs de la CGM et entraîner une surdose d'insuline susceptible d'entraîner une hypoglycémie sévère, et qui ne disposent pas d'une ouïe et/ou d'une vue suffisantes pour reconnaître toutes les fonctions du système Omnipod 5, y compris les alertes, les alarmes et les rappels. Les composants de l'appareil, notamment le Pod, le transmetteur et le capteur de CGM, doivent être retirés avant toute imagerie par résonance magnétique (IRM), tomodensitométrie (TDM) ou diathermie. De plus, le contrôleur et le smartphone doivent être placés hors de la salle d'intervention. L'exposition à l'IRM, à la TDM ou à la diathermie peut endommager les composants.
- Consultez le guide d'utilisation du système automatisé d'administration d'insuline Omnipod 5 pour obtenir la liste complète des indications, contre-indications, avertissements, mises en garde et instructions. Vous pouvez obtenir ce guide en nous appelant au 1-855-POD-INFO (1-XNUMX-POD-INFO).855-763-4636) ou en visitant notre website à omnipod.com
- ©2025 Insulet Corporation. Omnipod et le logo Omnipod sont des marques commerciales ou des marques déposées d'Insulet Corporation aux États-Unis et dans d'autres juridictions. Tous droits réservés. Toutes les autres marques commerciales appartiennent à leurs détenteurs respectifs. L'utilisation de marques tierces ne constitue pas une approbation et n'implique aucune relation ou affiliation.
- Insulet Corporation, 1540, chemin Cornwall, bureau 201, Oakville (Ontario) L6J 7W5. INS-OHS-12-2024-00217 V1.0
Questions fréquemment posées
- Q : Qui devrait utiliser ce système d’administration automatisée d’insuline sans tube ?
- R : Ce système est conçu pour les très jeunes enfants atteints de diabète de type 1 sous la supervision de professionnels de la santé.
- Q : Quels sont les principaux objectifs de l’utilisation de ce système ?
- A : Les principaux critères d’évaluation comprennent l’évaluation des niveaux d’HbA1c à la fin de la phase AID par rapport à la valeur initiale et la comparaison des taux d’incidence d’hypoglycémie sévère ou d’acidocétose diabétique avec le traitement standard.
- Q : Quelle est la durée de la période d'étude pour utiliser cet appareil ?
- R : L’étude comprend une phase de thérapie standard de 14 jours suivie d’une phase AID de 3 mois avec le système Omnipod 5.
Documents / Ressources
 |
Système automatisé d'administration d'insuline Omnipod [pdf] Manuel du propriétaire Système automatisé d'administration d'insuline, système d'administration d'insuline, système d'administration |
